- Study on Electron Beam Irradiation Dose Prediction Method for the Synthesis of Gold Nanoparticles Stabilized with Polymers
Hong-Ki Choi, In-Tae Hwang, Junhwa Shin, Jong-Hyun Jung, Hyun-Bin Kim, and Chan-Hee Jung†

Advanced Radiation Technology Institute, Korea Atomic Energy Research Institute, Jeongeup, Jeollabuk-do 56212, Korea
- 고분자로 안정화된 금 나노입자 합성을 위한 전자선 조사 선량 예측방법 연구
한국원자력연구원 첨단방사선연구소
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
This study aimed to develop a Geant4-DNA-based dose prediction method for the efficient and size-controllable electron beam-induced synthesis of gold nanoparticles (AuNPs) stabilized with polymers, and to analyze factors influencing their sizes. The required dose for the complete reduction of 0.5 mM HAuCl4 precursors was predicted using the computational G-values representing yields of chemical species formed from electron beam radiolysis of water, and compared with measured values. The UV-vis and TEM results revealed that both polymer stabilizer and dose rate act as reaction factors directly influencing the plasmon resonance bands and sizes of AuNPs synthesized by electron beam irradiation.
본 연구에서는 전자선 조사를 통해 제조하는 금 나노입자의 크기와 조사 선량과의 상관 관계를 예측하기 위해 Geant4-DNA 전사모사 방법을 고안하였다. 물의 전자선 분해로 생성되는 화학종의 수득율인 G값 산출을 통해 0.5 mM HAuCl4 전구체의 완전한 환원에 요구되는 선량을 전산모사 방법으로 예측하였고 이를 실험 측정값과 비교하였다. 전자선을 이용하여 합성된 금 나노입자의 UV-vis와 TEM 분석 결과, 고분자 안정화제와 조사 선량율이 금 나노입자의 플라스몬 공명 밴드와 나노입자 크기에 직접적인 영향을 주는 반응 인자로 작용함을 확인하였다.
A dose prediction method for the electron beam-induced synthesis of gold nanoparticles (AuNPs) with polymer stabilizers was developed. The dose for the complete reduction of 0.5 mM precursors was predicted based on the G-values of formed reducing species from water radiolysis, and compared with measured values. Both polymer stabilizer and dose rate acted as reaction factors directly influencing the plasmon resonance bands and sizes of AuNPs.
Keywords: gold nanoparticles, electron beam-induced radiolysis, dose prediction, polymer stabilizer, dose rate.
본 연구는 한국원자력연구원의 주요사업의 지원을 받아 수행되었습니다(과제번호 523620-25).
저자(들)는 이해상충이 없음을 선언합니다.
금속 나노입자는 벌크 상태의 금속과는 다른 독특한 전기적, 광학적, 자기적 및 화학적 특성을 보여 지난 반세기 이상 동안 크게 발전해 왔으며 의∙생명공학, 전자공학, 촉매, 센서, 환경 등 다양한 분야에서 널리 응용되고 있다.1-3 이러한 독특한 특성은 입자 크기, 모양 및 구성성분에 의존하며, 이러한 요소들을 조절함으로써 응용 분야에서 요구되는 새로운 특성을 도출하거나 최적화할 수 있다.4,5 따라서, 금속 나노입자의 크기, 모양 및 조성 등을 쉽게 제어할 수 있으면서도 환경친화적이고 빠르게 합성할 수 있는 방법에 대한 연구가 활발하게 이루어지고 있다.6-8
금속 나노입자의 합성은 물리적이나 화학적 방법으로 이루어지고 있다.9,10 물리적 방법은 큰 물질을 작은 단위로 세분화하는 하향식이 사용되며, 금속 이온을 환원제나 방사선을 이용하여 환원시키는 화학적 방법은 화학 반응으로 생성된 금속 원자가 입자로 응집되도록 하는 상향식이 주를 이루고 있다. 일반적으로 화학적 방법은 물리적 방법과 비교하여 반응 조절이 쉽고 낮은 비용으로 작고 균일한 나노입자의 대량 생산이 가능하며 표면 개질이나 기능화가 용이한 장점이 있다.11,12 화학적 방법으로 금속 나노입자를 제조할 경우 금속이온을 환원시키는 환원제(reducing agent) 외에도 환원된 금속 원자의 응집 거동을 제어할 수 있는 안정화제(stabilizer)를 첨가하는 것이 필요하다. 이러한 안정화제는 금속 나노입자 표면에 흡착하여 구연산과 같은 단분자에 의한 입자간 정전기적 반발력을 주거나 polyvinyl alcohol(PVA)과 polyvinyl pyrrolidone(PVP)과 같은 고분자에 의한 입체적 장애를 통해 나노입자를 안정화한다.11,13,14 특히, 고분자 안정제의 경우 분자 리간드에 비해 나노입자 주위에 두꺼운 입체적 장벽을 형성하여 응집 억제 효과가 크고, 장기적 분산 안정성이 우수하다는 점에서 화학적 및 물리적 합성법 모두에서 널리 활용되고 있다.15
다양한 상향식 방법 중에서도 방사선을 이용한 금속 나노입자의 합성 방법은 고분자 안정화제와 금속 이온이 용해된 용액 상태에서 직접 방사선을 조사하여 나노입자를 합성하는 방법이다.16 이러한 합성법은 물의 방사선 분해 반응을 통해 생성되는 높은 환원력을 갖는 수화 전자와 환원 라디칼을 이용하기 때문에 유기산류, 알코올류, 또는 수소화붕소나트륨이나 하이드라진과 같은 유해한 화학약품을 사용하는 화학적 방법과 비교하여 상온에서 빠르게 대량으로 나노입자를 형성할 수 있다. 또한, 조사 선량 및 선량율 등의 방사선 조사 조건을 조절함으로써 나노입자의 크기와 형상을 쉽게 제어할 수 있는 장점이 있어 친환경적이고 효율적인 방법으로 주목받고 있다.17,18 이러한 이점을 활용하여 감마선, 전자선 및 엑스선과 같은 방사선을 이용한 단일 금속이나 합금 나노입자의 합성 연구가 활발하게 이루어지고 있다.19,20 하지만, 지금까지의 연구 방법은 시행착오를 통해 얻어지는 경험을 기반으로 금속 나노입자 전구체의 환원 반응에 필요한 선량 예측 없이 이루어지고 있으며, 이러한 연구 방식은 비효율적인 에너지 사용과 시간 낭비 문제를 초래할 수 있다. 따라서 효율적인 방사선 합성을 위해 조사량을 예측하고 최적화할 수 있는 새로운 방법론이 요구된다.
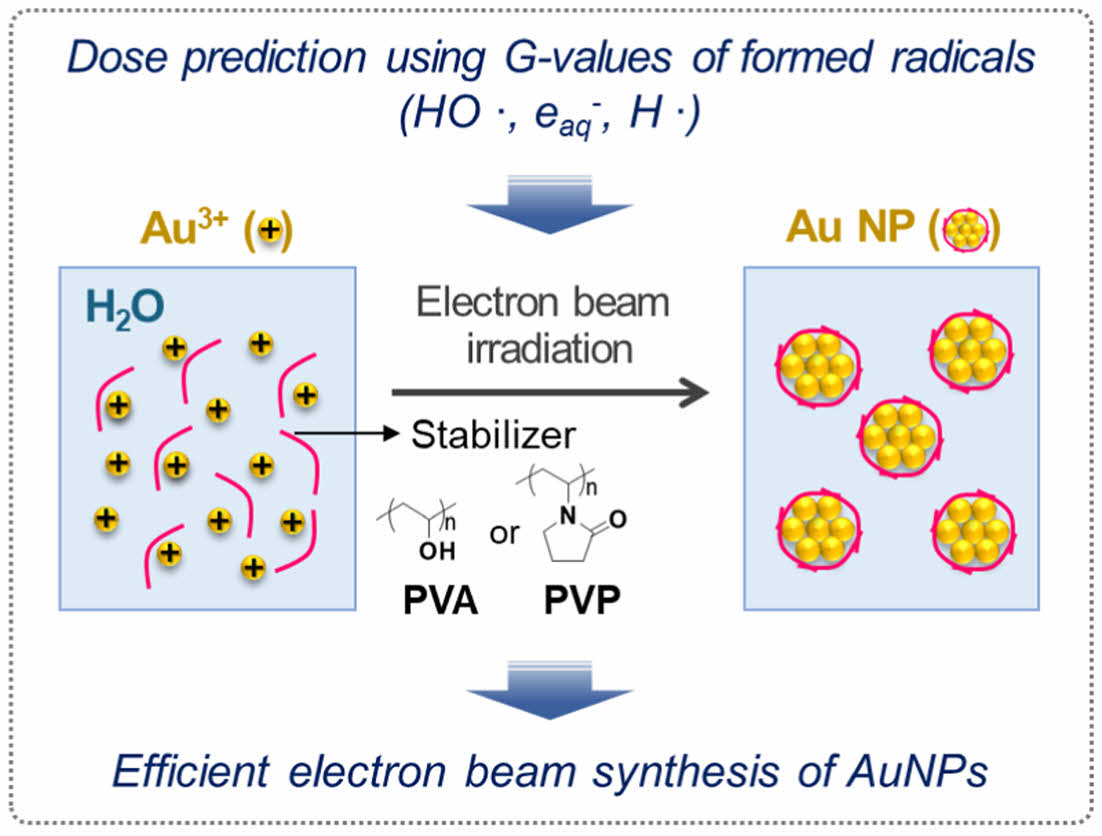
Geant4-DNA는 개방형 Geant4의 확장 버전으로 방사선의 생물학적 영향을 상세히 모델링할 수 있도록 설계된 몬테카를로 전산모사 도구이다.21,22 이를 통해 생물학적 영향의 핵심적인 부분을 차지하는 물의 이온화 방사선 분해를 전산모사하고, 100 eV의 흡수된 에너지당 화학종의 수를 의미하는 G값을 계산하는데 활용할 수 있다.23 따라서, Geant4-DNA를 이용한 G값의 산출을 통해 물의 분해 과정에서 생성되는 수화 전자(eaq-), 수소라디칼(H‧), 수산화라디칼(HO‧) 등의 화학종을 정량화함으로써 특정 금속 나노입자 전구체 농도에서 환원 반응의 종결에 필요한 선량 예측이 가능하다. 이에, 본 연구에서는 전자선을 이용한 금 나노입자의 합성(Scheme 1)을 위한 선량 예측 방법을 제시하고 금 나노입자의 크기에 미치는 영향 인자를 분석하고자 하였다.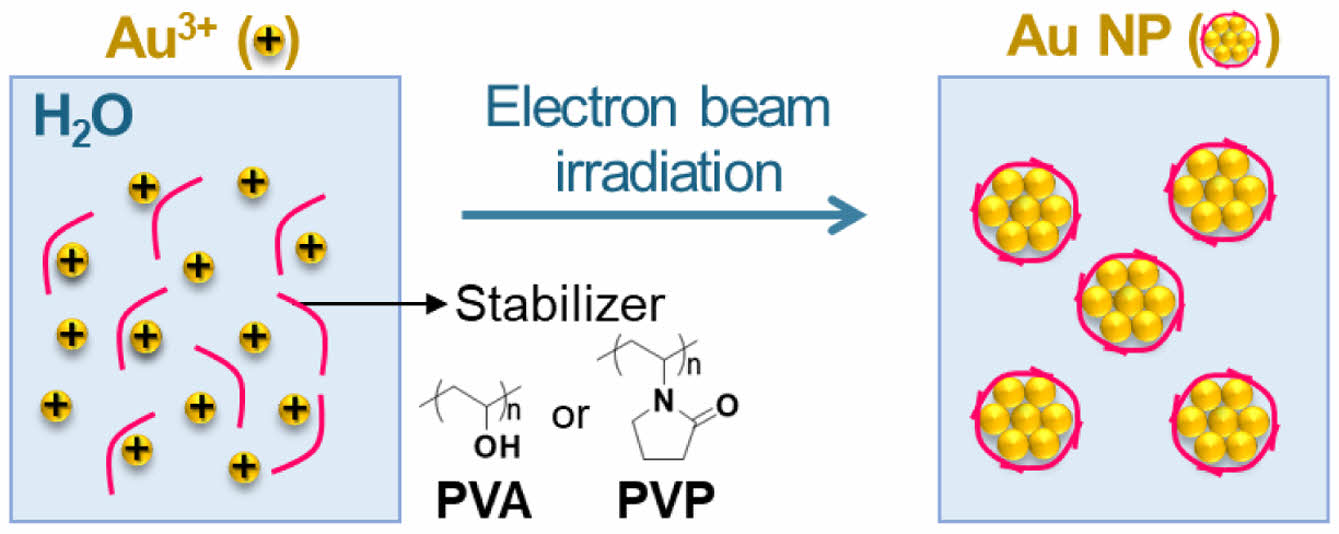
Scheme 1. Electron beam-induced synthesis of gold nanoparticles
(Au NP) with polymer stabilizers.
재료. 금 나노입자의 전구체로는 hydrogen tetracholroaurate (HAuCl4, ³99.9%, Kojima, Japan)를 사용하였고 고분자 안정화제로는 PVA(polyvinyl alcohol, MW 85k~124k, Merck, USA)와 PVP(polyvinyl pyrrolidone, MW 630k, Merck, USA)를 사용하였으며 라디칼 제거제로는 이소프로판올(isopropanol (iPrOH), ≥99.%, Merck, USA)을 이용하였다.
Geant4-DNA 전산모사 이용 물의 전자선 분해 과정에서의 생성되는 반응성 화학종의 G값 산출. 물의 전자선 분해로부터 생성되는 반응성 화학종의 수인 G값을 계산하기 위해 개방형 Geant4-DNA의 공개 버전(11.2.2)과 최근 구현된 독립 반응 시간(independent reaction time, IRT) 기법(Example-chem6에서 제공)을 사용하였다. Geant4-DNA는 방사선(전자선, 감마선 등)과 물질(물 등) 간의 상호작용을 계산하는 몬테카를로 기반 전산모사 도구로, 방사선의 물리적 에너지 전달 과정부터 생성 화학종의 확산 및 화학반응에 이르는 다단계 공정을 구현할 수 있다.22,23 전산모사의 주요 조건은 다음과 같다. 먼저, 물의 3차원적 구조는 1.5 μm 반지름의 구형으로 구성하였다. 해당 체적을 갖는 구형으로 설정한 이유는 전자와 물 분자 간의 주요 물리적 충돌이 반응 구 내에서 충분히 발생하도록 하면서도 전산모사에 필요한 충분한 양의 화학종을 생성할 수 있는 체적이기 때문이다. 구형 모델의 크기가 증가하면 연산 과정이 증가하여 계산 시간 또한 증가하게 된다.24 방사선은 1 MeV의 운동에너지를 가지는 전자이며, 0.5~20 kGy 범위의 조사 선량에 해당하는 면적당 전자 수를 물의 구 면적으로 환산한 값인 1344(0.5 kGy), 2507(1 kGy), 4608(2 kGy), 8811 (4 kGy), 10913(5 kGy), 17217(8 kGy), 21242(10 kGy) 및 41667 (20 kGy)의 조건에서 각각 전산모사를 수행하였다. 적용된 IRT 기법은 물의 방사선 분해로 생성된 반응성 화학종의 시간-공간적 확산 및 재결합 과정을 개별적으로 추적하며, 각 반응의 확산 계수와22 속도 상수를23 반영하여 실제 화학 반응이 진행되는 과정을 동적으로 재현한다. 최종적으로 전산 모사로 도출된 시간에 따른 생성된 반응성 화학종의 G값 변화가 안정화되는 시점인 10 ns에서의 G값을 평균값으로 사용하였다.
전자선 환원 반응의 종결에 필요한 선량 예측. 상기 산출된 G값을 활용하여 식 (1)을 통해 단위 선량당 생성 환원 라디칼 농도[C, mol/L]를 계산하였다.

이때 D는 사용된 전자선 선량(kGy)으로 1 kGy를 1000 J/kg로 변환한 값이고 G'는 Geant4-DNA 전산 모사로 얻어진 G(molecules/100 eV)값을 mol/J 단위로 변환한 값이며, ρ는 수용액의 밀도(kg/L)를 의미하며, 본 연구에서 사용된 금 나노입자의 전구체 농도가 0.01 M 이하로 낮아 물의 밀도 값인 1 kg/L의 값을 사용하였다.25 HAuCl4 전구체 수용액의 경우에는 단위 선량당 환원종(reducing species)의 농도를 eaq-와 H‧의 농도의 합으로 계산하였다. iPrOH을 첨가한 경우 iPrOH과 라디칼(H‧과 HO‧)과의 반응으로 iPrOH 라디칼((CH3)2C‧OH, iPrOH‧)이 생성되어 환원제로 작용하므로 단위 선량당 환원종(reducing species)의 농도를 eaq-, H‧ 및 HO‧ 농도의 합으로 계산하였다. 최종적으로 산출된 단위 선량당 생성 환원종 농도를 활용하여 식 (2)를 통해 특정 0.5 mM의 금 나노입자 전구체 농도에서 환원 반응의 종결에 필요한 선량 예측을 위한 추정 전환율(calculated conversion rate)을 산출하였다.
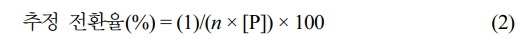
여기서 n은 금속 이온의 산화수(금 이온의 경우 3)이며, P는 환원 반응에 사용한 금 나노입자 전구체의 몰농도[mol/L]를 나타낸다.
금 나노입자의 전자선 합성. 선량에 따른 금 나노입자의 전구체의 전환율 측정을 위해 HAuCl4 전구체를 증류수에 용해한 0.5 mM의 HAuCl4 수용액과, 400 mM의 iPrOH 라디칼 제거제와 50 mM의 PVA 또는 PVP 안정화제를 함유한 0.5 mM의 HAuCl4 수용액을 각각 제조하였다. 제조된 전구체 수용액을 50 mL의 유리병에 넣고 고무마개로 밀폐한 다음 산소에 의한 부반응이 없는 환경 조성을 위해 질소로 30분간 충전하였다. 이후 금 나노입자의 합성을 위해 정읍 첨단방사선연구소에 설치된 2.5 MeV 전자가속기를 이용하여 1 MeV의 가속에너지와 1 kGy/s의 고정 선량율로 1-12 kGy의 선량을 상기 질소로 충전된 유리병에 조사하였다. 제조된 금 나노 입자는 IPA와 PVA 첨가의 유무에 따라 NO-X와 iPrOH-X로 표기하였고 X는 선량을 나타낸다. PVA와 PVP 안정화제에 따른 금 나노입자의 합성을 위해 1 kGy/s의 고정 선량율로 10 kGy의 선량을 조사하였고 PVA-10과 PVP-10으로 명명하였다. 선량율에 따른 금 나노입자의 합성을 위해 10 kGy/s과 20 kGy/s의 선량율로 각각 10 kGy와 20 kGy의 선량을 조사하였고 선량율에 따라 PVA-r10 과 PVA-r20으로 명명하였다.
금 나노입자 전구체의 전환율 측정. 선량에 따른 전환율 정량화를 위해서 0.1, 0.25, 0.5, 0.75 및 1.0 mM의 금 나노입자 전구체(HAuCl4) 농도에서 313 nm 파장의 흡광도를 측정하여 Beer-Lambert 법칙을 수렴하는 선형 검량곡선(r = 0.9983)을 확보하였고 이를 통해 전자선 조사 후 미반응 나노입자 전구체의 농도(X)를 산출하는 방정식을 도출하였다.26
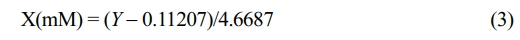
여기서 Y는 313 nm의 파장에서 측정된 전자선 조사된 금 나노입자 전구체 용액의 흡광도(absorbance)를 나타낸다. 이후 수식(4)를 통해 선량에 따른 금 나노입자 전구체의 측정 전환율(measured conversion rate)을 산출하였다.
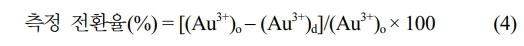
여기서 (Au3+)o와 (Au3+)d는 각각 특정 조사량에서의 전자선 조사 전·후의 금 나노입자 전구체의 몰농도[mol/L]를 나타낸다.
생성된 금 나노입자의 특성 분석. 용액의 사진은 스마트폰(Galaxy S24)으로 촬영하였고, 광학적 특성은 UV-Vis 분광기(Mega-900, Scinco, Korea)를 활용하여 분석하였다. 나노입자 크기 및 선택영역회절패턴(selected area electron diffraction, SAED)은 투과전자현미경(FE-TEM, Tecnai G2 F30 S-Twin, FEI, Japan)을 이용해 분석하였고, 크기 분포도는 DigitalMicrograph (Gatan, USA) 소프트웨어를 이용해 분석하였다.
전자선을 금 이온이 녹아 있는 증류수에 조사하면 물의 분해로 eaq-, H·, HO·, H2, H2O2 등의 다양한 화학종이 생성된다.23,27 이후 금 이온(Au3+)의 환원 반응은 전자선의 직접적인 반응이 아닌 물의 분해로 생성된 강력한 환원제인 수화 전자(eaq-)와 수소라디칼(H·)에 의해 이루어진다. 또한, 생성된 수산화라디칼(HO·)은 매우 강한 산화제로서 금 이온이나 새로 형성된 금 원자(Au0)를 산화할 수 있어 환원 반응의 효율을 저하시킬 수 있다. 이를 막기 위해 일반적으로 이소프로판올(iPrOH)과 같은 알코올을 첨가하면 수산화라디칼과 수소라디칼은 이소프로판올과 반응하여 사라지면서 환원제로 작용할 수 있는 이소프로판올 라디칼(iPrOH‧, (CH3)2C‧OH)이 생성된다.28 eaq-, H·, iPrOH‧과 같은 환원종(reducing species)은 금 이온을 신속하게 환원할 수 있는 높은 환원력을 가지며 이의 생성 농도는 선량(absorbed dose)에 의존한다. 본 연구에서는 금 나노입자의 효율적인 전자선 합성을 위해, Geant4-DNA를 이용해 환원에 참여하는 전자와 라디칼의 농도를 정량화함으로써 특정 금 나노입자 전구체 농도에서 환원 반응을 종결하는 선량을 예측하는 방법을 연구하였다.
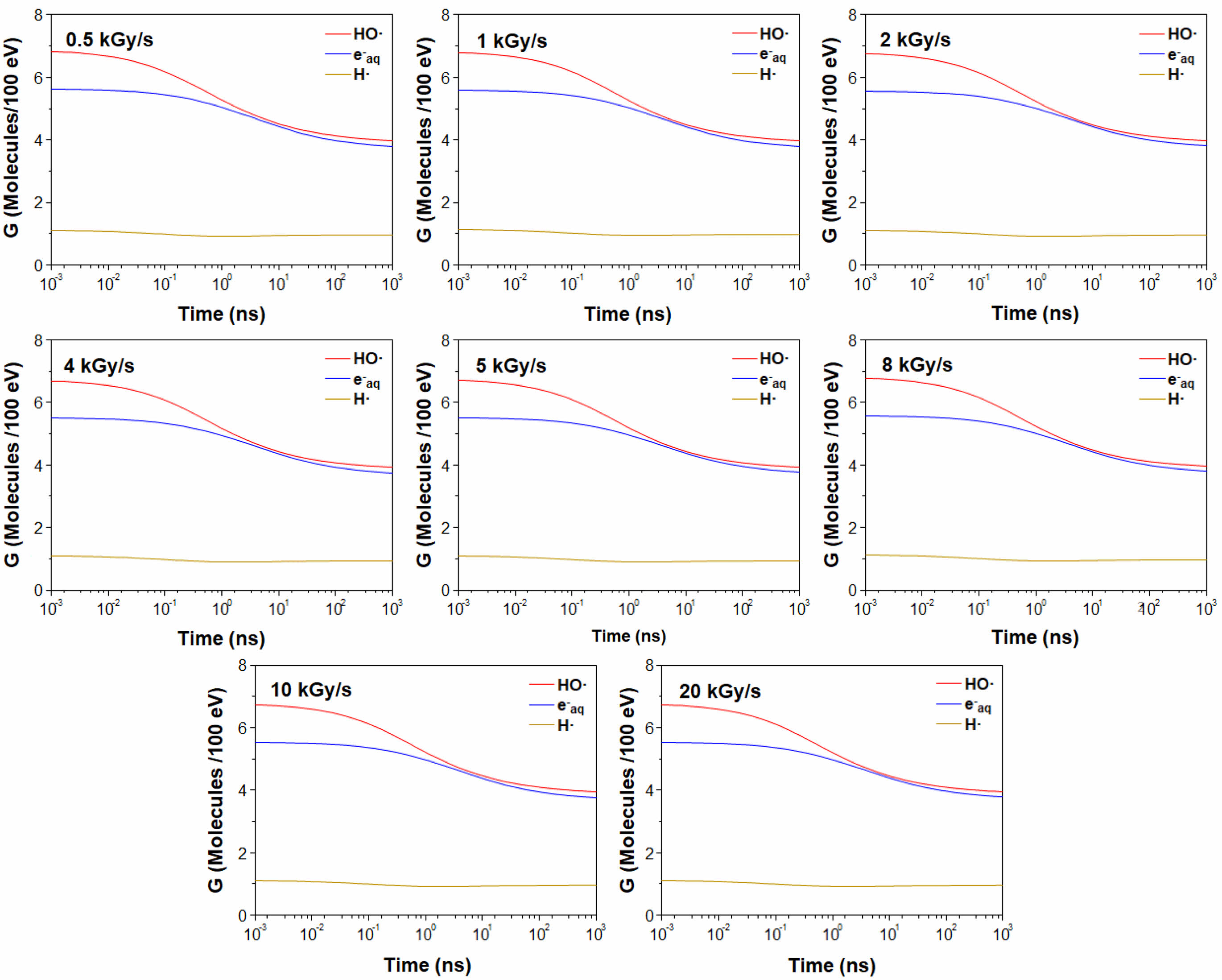
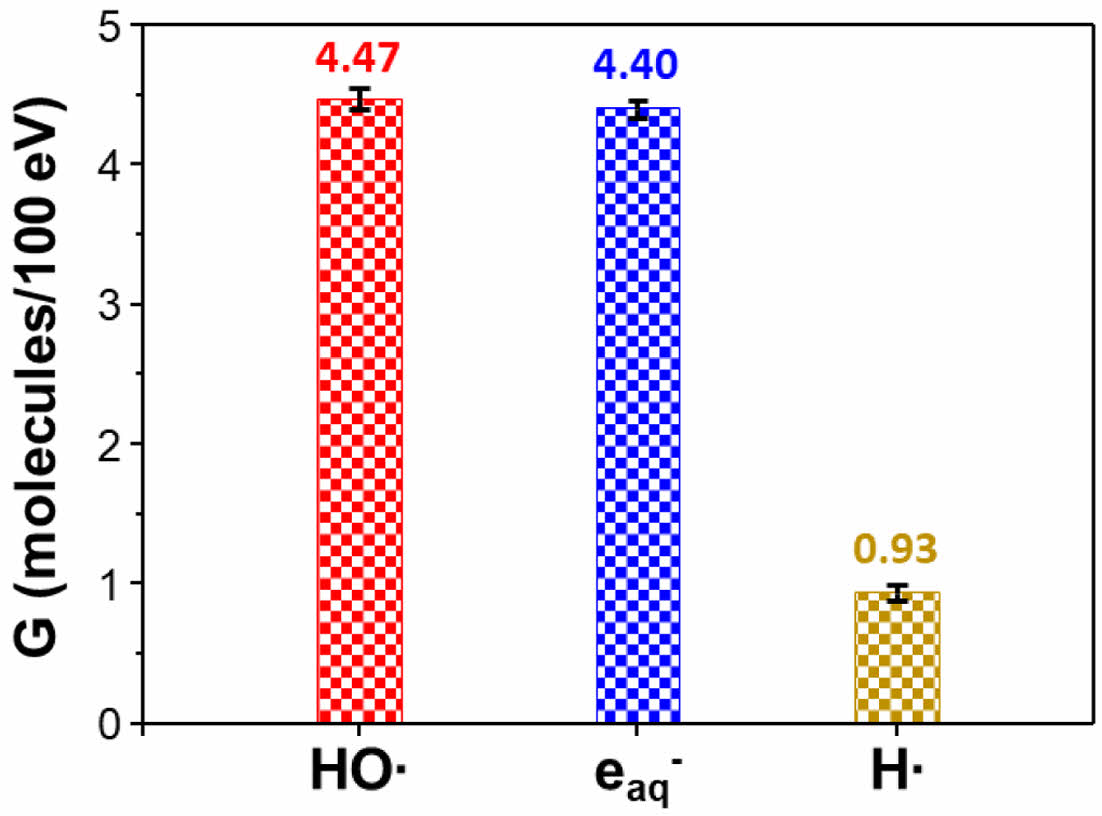
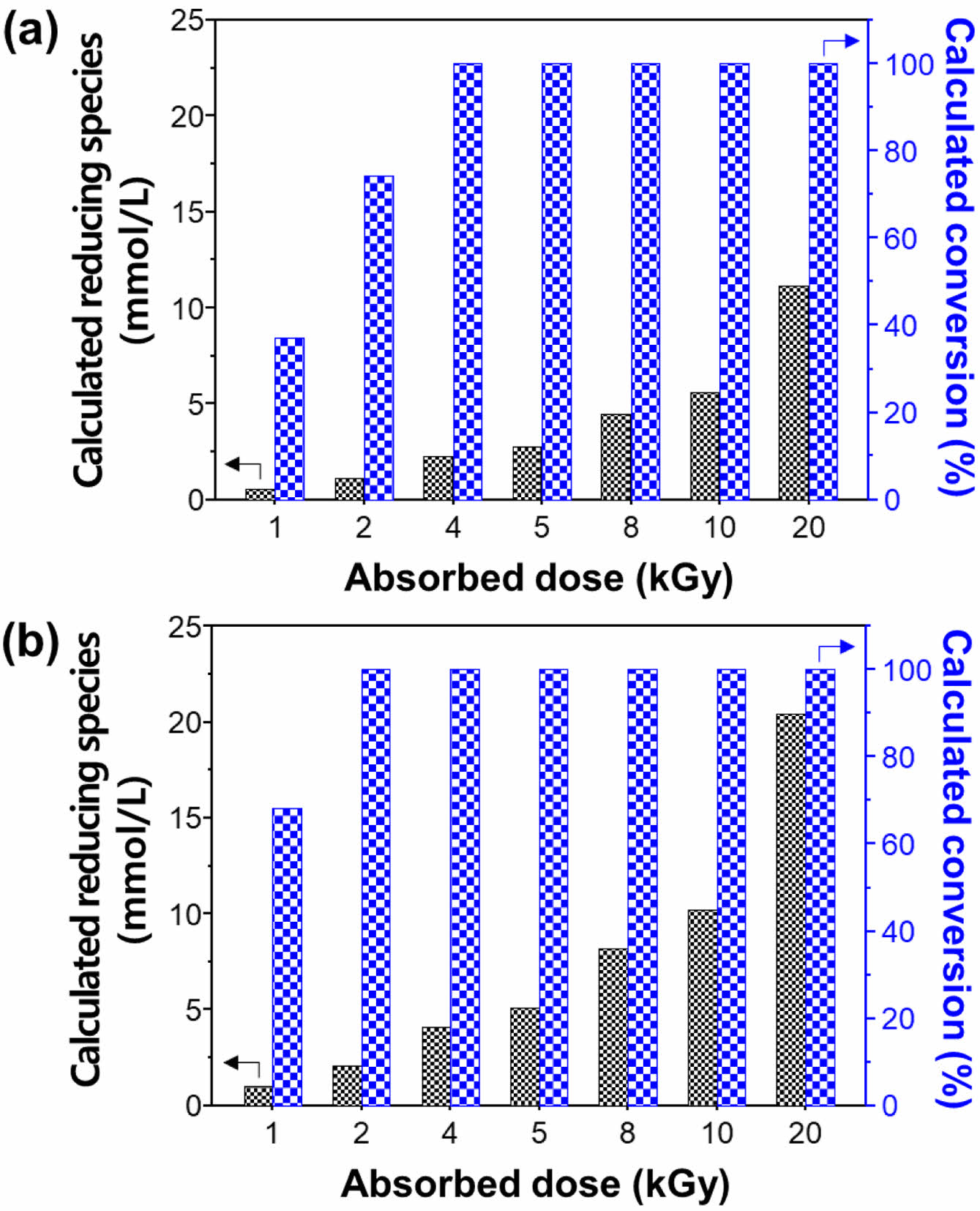
Geant4-DNA 전산모사로부터 도출된 다양한 선량에서 시간에 따른 HO‧, eaq- 및 H‧의 G값 변화를 보여주는 결과를 Figure 1에 나타내었다. Figure 1은 주어진 모든 선량에서 HO‧, eaq- 및 H‧의 G값이 유사함을 보여주는데 이는 G값이 선형에너지전달능(linear energy transfer, LET)에 의해 결정되기 때문이다.29 전자선 조사에 의한 물 분해로 생성된 화학종 농도와 금 나노입자의 전구체의 전환율 계산을 위해, 값의 변화가 안정화되는 시점인 10 ns에서의 선량별 G값을 평균하여 Figure 2에 나타내었다. HO‧, eaq- 및 H‧의 평균 G값은 각각 4.47, 4.40 및 0.93이었다. 이러한 결과를 기반으로 특정 0.5 mM 농도의 HAuCl4 전구체 용액에 대해 선량과 iPrOH 첨가 유무에 따른 환원종 농도와 추정 전환율을 예측한 결과를 Figure 3에 제시하였다. Figure 3(a)의 iPrOH이 없는 조건에서 생성된 환원종의 농도가 선량에 의존하며 0.5 mM 농도의 HAuCl4 전구체 용액의 환원 반응 종결을 위해 필요한 최소 선량이 그래프에서 100%의 추정 전환율을 보이는 4 kGy임을 확인하였다. Figure 3(b)의 iPrOH을 첨가한 조건에서는 생성된 환원종의 농도가 iPrOH이 없는 경우 대비 주어진 모든 선량에서 약 2배로 증가함에 따라 예측된 최소 선량이 2 kGy로 낮아짐을 보였다. 이러한 예측된 종결 선량의 감소는 앞서 언급한 바와 같이 eaq-의 G값과 유사한 수치를 보이는 산화제 HO·이 H·와 함께 iPrOH과 반응하여 (CH3)2C‧OH 라디칼 환원종으로 변환되면서 환원 반응의 효율이 전체적으로 증가했기 때문이다.30
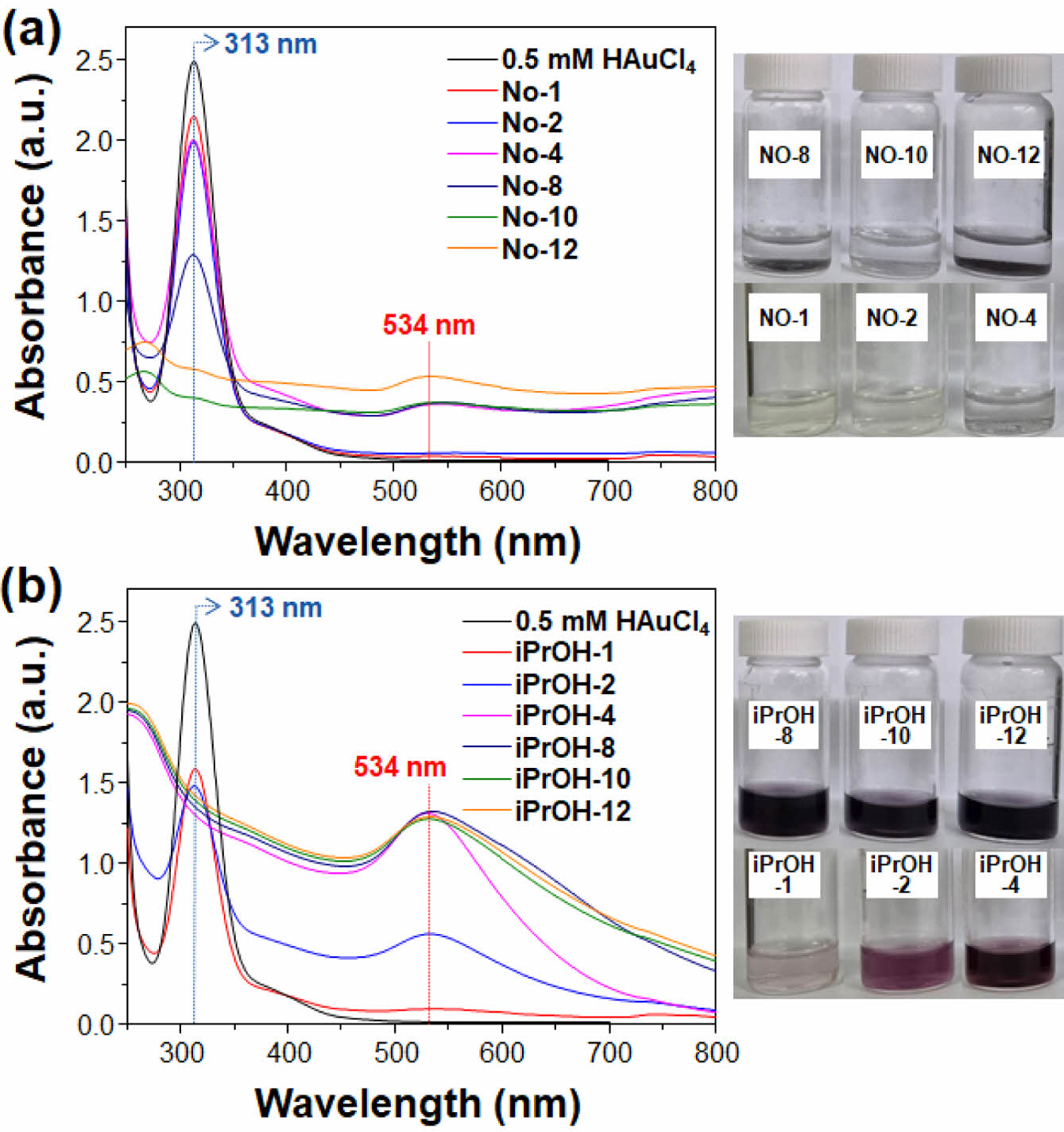
금 나노입자의 전자선 합성을 위해 요구되는 최소 선량을 측정하기 위해 다양한 선량에서의 iPrOH 첨가 유무에 따른 0.5 mM HAuCl4 전구체 용액의 환원반응을 진행하였다. Figure 4(a)의 UV-vis 스펙트럼과 광학 사진에서 나타난 바와 같이, iPrOH과 PVA 안정화제가 없는 HAuCl4 전구체 용액인 No-X 샘플에서는 10 kGy 이상의 조사 선량에서 HAuCl4 전구체에 해당하는 313 nm의 흡광 밴드가 소멸되었다. 이러한 결과로부터 10 kGy 이상의 선량에서 미반응 전구체 없이 환원 반응이 종결됨을 확인할 수 있다. 또한, 광학 사진에서 보는 바와 같이 생성된 금 나노입자는 침전 상태로 존재하는데 이는 안정화제 첨가 없이는 생성된 나노입자가 높은 표면 에너지로 인해 열역학적으로 불안정하고 반데르발스힘과 같은 입자 간의 인력으로 인해 나노입자 간의 응집과 합체가 일어나 침전되기 때문이다.14 반면, Figure 4(b)에서 보는 바와 같이, iPrOH과 PVA 고분자 안정화제가 첨가된 샘플(iPrOH-X)의 UV-vis 스펙트럼에서는 iPrOH이 첨가되지 않은 샘플(No-X) 보다 낮은 4 kGy의 선량에서 313 nm의 흡광 밴드가 소멸되어 환원 반응이 종료됨을 확인하였다. PVA 고분자 안정화제 첨가로 인해 금 나노입자는 침전 없이 잘 분산된 콜로이드 상태로 존재하며 금 나노입자의 특성 피크인 534 nm에서 플라스몬 공명(plasmon resonance) 흡광 밴드를 잘 보여준다.20
다양한 선량에서 iPrOH 첨가 여부에 따른 0.5 mM HAuCl4 전구체 용액의 측정 전환율과 추정 전환율을 Figure 5에 비교하여 나타내었다. iPrOH과 PVA 안정화제가 없는 HAuCl4 전구체 용액인 No-X 샘플에서는 환원 반응의 종결을 의미하는 100% 측정 전환율이 식 (2)를 통해 계산된 100% 추정 전환율 값인 4 kGy의 선량에 비해 다소 높은 10 kGy로 확인되었다. 하지만, iPrOH-X 샘플에서는 No-X 샘플에 비해 최소 선량이 4 kGy로 감소하였고 2 kGy로 계산된 선량과의 차이도 감소하였음을 확인하였다. 이러한 차이는 Geant4-DNA에서 전산 모사할 수 있는 규모(scale)의 한계 때문으로 여겨지며 계산 규모를 확장하고 입력 데이터를 추가할 경우 실제 측정 값과 근접한 값을 보여줄 것으로 예상된다. 또한, 본 연구의 전자선 선량 예측 방법은 대부분 금속 이온을 환원시킬 수 있을 정도의 강력한 환원력을 갖는 수화 전자와 환원 라디칼을 기반으로 하기 때문에 금 이외에도 은, 구리, 백금 등을 포함한 금 속 나노입자의 합성에도 적용할 수 있을 것으로 기대된다.
iPrOH의 첨가에 따른 금 나노입자 전구체 수용액에서의 전자선 환원 반응의 효율 향상에 대한 잠정적인 메커니즘을 Figure 6에 나타내었다.31 메커니즘에 제시된 바와 같이 iPrOH ((CH3)2CHOH)이 첨가되면 반응식 (i)의 전자선 물 분해(radiolysis)에 의해 생성된 H·와 HO·가 반응식 (ii)에 따라 (CH3)2C‧OH가 생성되어 eaq-와 함께 환원제로 작용한다. 이러한 과정으로 특정 선량에서 생성되는 환원종의 양은 Figure 2의 결과에서 기술한 바와 같이(CH3)2C‧OH이 eaq-와 유사한 양의 ‧OH와 ‧H와 함께 반응하여 생성되므로 iPrOH이 없는 조건 대비 약 2배 정도로 증가한다. 이로 인해서 반응식 (iii), (iv), (v) 및 (vi)에 따라 eaq-와 (CH3)2C‧OH에 의해 Au3+가 Au2+로 환원된 후 Au2+ 이온은 불균등화(disproportionation) 반응에 의해 Au3+와 Au1+가 형성되고 Au1+는 추가적인 반응을 통해 Au0로 환원이 이루어진다. 하지만 iPrOH이 첨가되지 않을 시에는 같은 선량에서 생성된 환원종의 양이 적어 반응식(vi)에 의한 Au1+의 환원 반응이 어려워 더 높은 선량이 요구된다. 이후 형성된 Au0 는 반응식 (vii), (viii) 및 (ix)에 따라 이합체화 (dimerization), 응집(aggregation) 및 합체(coalescence) 과정을 통해 염화물 음이온(chloride anions)으로 둘러싸인 더 높은 핵성(nuclearity)을 가진 핵을 생성하고, 생성된 핵은 나노입자로 성장하는 것으로 추정된다.
금 나노입자의 전자선 합성에 고분자 안정화제의 종류와 선량율이 미치는 영향을 조사하기 위해 0.5 mM 전구체의 측정 전환율이 100%를 보이는 선량의 조건에서 생성된 금 나노입자의 광학적 및 형태학적 특성을 UV-vis와 TEM을 이용하여 분석하였고, 그 결과를 각각 Figure 7과 8에 나타내었다. Figure 7(a)의 UV-vis 스펙트럼에서 나타난 바와 같이, 1 kGy/s의 선량율로 10 kGy의 선량을 조사하여 제조된 PVA-10과 PVP-10 샘플은 모두 금 나노입자의 플라스몬 공명에 의해 나타나는 흡광 밴드를 보였으나, PVP-10의 흡광 밴드 파장은 534 nm에 나타나는 PVA 샘플의 플라스몬 흡광 밴드 파장에 비해 상대적으로 짧은 527 nm에서 나타났다. 이러한 파장의 차이는 이전 문헌에서 보고된 바와 같이 생성된 금 나노입자의 크기 차이에 기인한 것으로 PVP 안정화제가 첨가된 환경에서 더 작은 크기의 금 나노입자가 생성되었음을 의미한다.32 또한, Figure 7(b)의 TEM 사진, 선택영역전자회절(selected area electron diffraction, SAED) 패턴 및 크기(size) 분포도에서 볼 수 있듯이, PVA-10과 PVP-10은 모두 결정성 금 나노입자가 생성되었음을 의미하는 선택영역전자회절 패턴을 보였지만 평균(mean) 입자 크기는 각각 6.13±1.23 nm와 4.90±1.30 nm로 차이를 보였다. 이러한 결과는 PVP 안정화제의 작용기와 금 나노입자 간의 상호작용 세기가 PVA 안정화제에 비해 크기 때문이며 고분자 안정화제가 금 나노입자의 크기와 크기 분포도에 직접적인 영향을 미치는 요소임을 보여준다.33
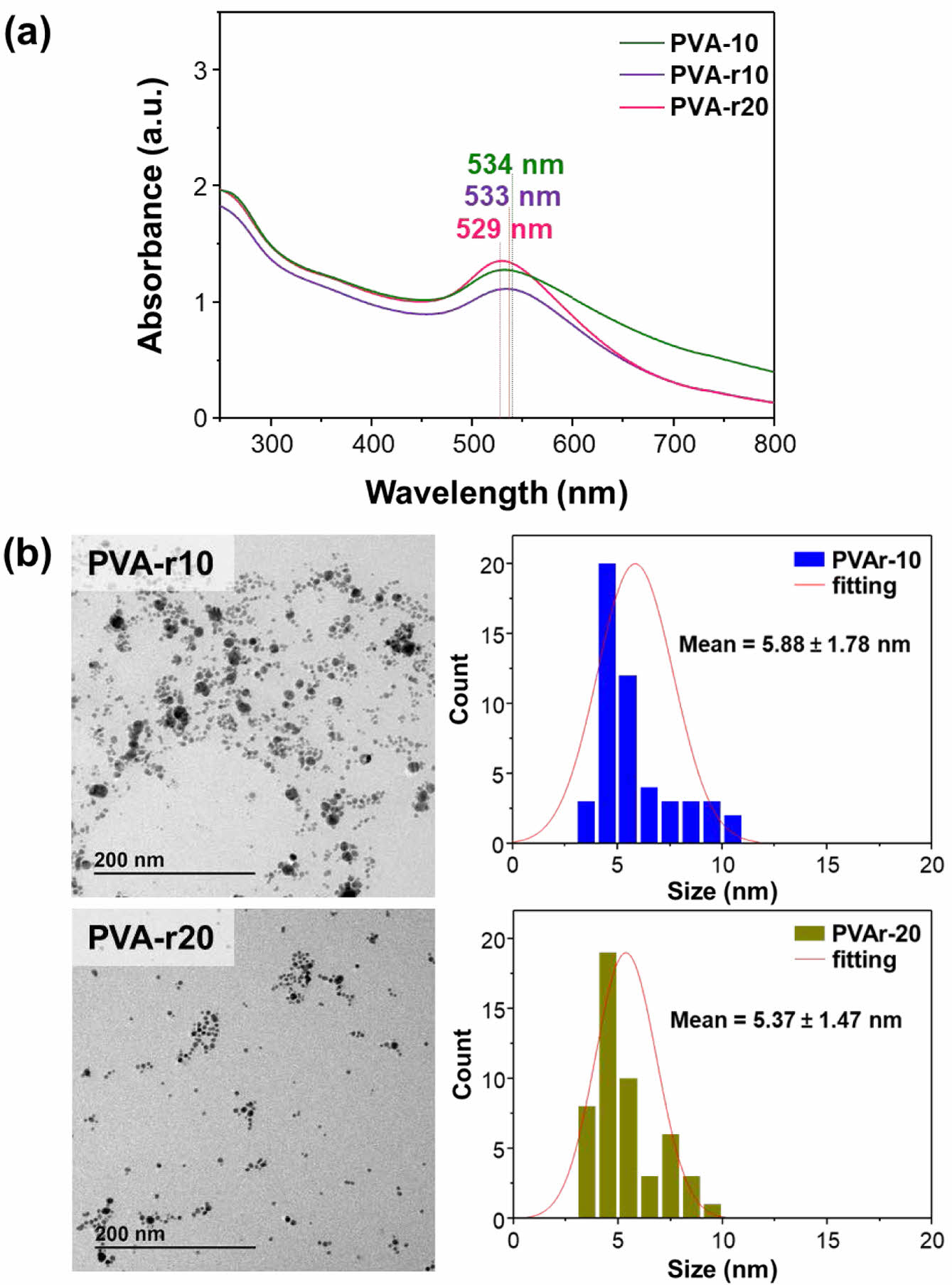
Figure 8(a)의 UV-vis 스펙트럼에서는 10 kGy/s와 20 kGy/s의 선량율로 10 kGy와 20 kGy의 선량을 조사하여 제조된 PVA-r10과 PVA-r20 샘플 모두 PVA-10 샘플과 같이 플라스몬 공명 밴드를 보였으나, 흡광 밴드의 파장은 각각 PVA-10 보다는 다소 짧은 533 nm와 529 nm에서 관찰되었다. 또한, Figure 8(b)의 TEM 크기 분포도에서도 PVA-r10과 PVA-r20 샘플의 크기 가 선량율이 증가함에 따라 6.13±1.23 nm의 평균 PVA-10 샘플 크기에 비해 다소 작은 각각 평균 5.88±1.78 nm와 5.37±1.47 nm로 감소하였다. 이러한 결과는 선량율이 높을수록 생성되는 환원종의 양이 증가함으로 인해 다수의 핵이 빠르게 동시적으로 생성되기 때문이며 선량율도 금 나노입자의 크기 분포도에 영향을 미치는 직접적인 인자로 작용함을 보여준다.31
|
Figure 1 Time-evolution of G-values for hydroxyl radicals (HO·), hydrated electrons (eaq- ), and hydrogen radicals (H·) generated from 1 MeV electron beam-induced radiolysis of water at different doses calculated with Geant4-DNA simulation. |
|
Figure 2 Average G-values of hydroxyl radical (HO·), hydrated electron (eaq- ), and hydrogen radical (H·) taken at the time of 10 ns in Figure 1. |
|
Figure 3 Concentration of reducing species and corresponding conversion of 0.5 mM HAuCl4 at different absorbed doses calculated using the obtained G values: (a) without; (b) with iPrOH. |
|
Figure 4 UV-vis spectra and optical images of 0.5 mM HAuCl4 precursor solution irradiated with electron beams at absorbed doses of 1-12 kGy: (a) without; (b) with iPrOH. |

|
Figure 5 Measured conversion of 0.5 mM HAuCl4 precursor solution without (NO-X) and with iPrOH (iPrOH-X) as a function of absorbed dose and their corresponding 100% conversions calculated at the lowest absorbed dose from Figure 3. |

|
Figure 6 Tentative mechanism for the formation of gold nanoparticle trough electron beam-induced radiolysis of water with iPrOH. |

|
Figure 7 (a) UV-vis spectra; (b) TEM images, selected area electron diffraction (SAED) patterns, and size distribution of PVA-10 and PVP-10 prepared using 0.5 mM HAuCl4 precursor solution containing different polymer stabilizers under the fixed irradiation condition of 10 kGy and 1.0 kGy/s. |
|
Figure 8 (a) UV-vis spectra; (b) TEM images and size distribution of PVA-10, PVA-r10, and PVA-r20 prepared through irradiation at different dose rate of 1, 10, 20 kGy/s under the fixed 0.5 mM HAuCl4 precursor solution containing a PVA polymer stabilizer. |
본 연구에서는 Geant4-DNA 전산 모사로 산출된 물의 전자선 분해로 생성되는 화학종의 평균 G값을 이용하여 iPrOH의 첨가 유무에 따른 0.5 mM 금 나노입자 전구체의 완전 환원을 위해 필요한 최소 선량을 예측하고 측정값과 비교하였다. 전산 모사할 수 있는 규모와 입력 데이터의 제약으로 인해 예측된 선량과 측정된 선량 간에 다소 차이가 있지만 iPrOH의 첨가에 의한 최소 선량의 감소에 대한 동일한 경향성을 보임을 통해 금 나노입자의 효율적인 전자선 합성을 위한 선량 예측 방법으로의 활용 가능성을 확인하였다. 또한, PVA보다 PVP를 안정화제로 사용하거나 높은 선량율에서 상대적으로 작은 금 나노입자가 생성됨을 통해 고분자 안정화제의 종류와 선량율에 따라 전자선으로 제조되는 금 나노입자의 크기를 조절할 수 있음을 확인하였다.
- 1. Stark, W. J.; Stoessel, P. R.; Wohlleben, W.; Hafner, A. Industrial Applications of Nanoparticles. Chem. Soc. Rev. 2015, 44, 5793-5805.
-

- 2. Ndolomingo, M. J.; Bingwa, N.; Meijboom, R. Review of Supported Metal Nanoparticles: Synthesis Methodologies, Advantages and Application as Catalysts. J. Mater. Sci. 2020, 55, 6195-6241.
-

- 3. Draz, M. S.; Shafiee, H. Applications of Gold Nanoparticles in Virus Detection. Theranostics 2018, 8, 1985-2017.
-

- 4. García-Álvarez, R.; Hadjidemetriou, M.; Sánchez-Iglesias, A.; Liz-Marzán, L.M.; Kostarelos, K. In Vivo Formation of Protein Corona on Gold Nanoparticles. The Effect of Their Size and Shape. Nanoscale 2018, 10, 1256-1264.
-

- 5. Lopez-Chaves, C.; Soto-Alvaredo, J.; Montes-Bayon, M.; Bettmer, J.; Llopis, J.; Sanchez-Gonzalez, C. Gold Nanoparticles: Distribution, Bioaccumulation and Toxicity. In Vitro and In Vivo Studies. Nanomedicine 2018, 14, 1-12.
-

- 6. Jamkhande, P. G.; Ghule, N. W.; Bamer, A. H.; Kalaskar, M. G. Metal Nanoparticles Synthesis: An Overview on Methods of Preparation, Advantages and Disadvantages, and Applications. J. Drug Deliv. Sci. Technol. 2019, 53, 101174.
-

- 7. Dong, J.; Carpinone, P. L.; Pyrgiotakis, G.; Demokritou, P.; Moudgil, B. M. Synthesis of Precision Gold Nanoparticles Using Turkevich Method. Kona 2020, 37, 224-232.
-

- 8. Garibo, D.; Borbón-Nuñez, H. A.; De León, J. N. D.; García Mendoza, E.; Estrada, I.; Toledano-Magaña, Y.; Tiznado, H.; Ovalle-Marroquin, M.; Soto-Ramos, A. G.; Blanco, A.; Rodríguez, J. A.; Romo, O. A.; Chávez-Almazán, L. A.; Susarrey-Arce, A. Green Synthesis of Silver Nanoparticles Using Lysiloma Acapulcensis Exhibit High-Antimicrobial Activity. Sci. Rep. 2020, 10, 12805.
-

- 9. Ijaz, I.; Gilani, E.; Nazir, A.; Bukhari, A. Detail Review on Chemical, Physical and Green Synthesis, Classification, Characterizations and Applications of Nanoparticles. Green Chem. Lett. Rev. 2020, 13, 223-245.
-

- 10. Iravani, S.; Korbekandi, H.; Mirmohammadi, S. V.; Zolfaghari, B. Synthesis of Silver Nanoparticles: Chemical, Physical and Biological Methods. Res. Pharm. Sci. 2014, 9, 385-406.
- 11. Mirzaei, A.; Janghorban, K.; Hashemi, B.; Bonyani, M.; Leonardi, S. G.; Neri, G. Characterization and Optical Studies of PVP-Capped Silver Nanoparticles. J. Nanostructure Chem. 2017, 7, 37-46.
-

- 12. Sajid, M.; Płotka-Wasylka, J. Nanoparticles: Synthesis, Characteristics, and Applications in Analytical and Other Sciences. Microchem. J. 2020, 154, 104623.
-

- 13. Shiraishi, Y.; Tanaka, H.; Sakamoto, H.; Ichikawa, S.; Hirai, T. Photoreductive Synthesis of Monodispersed Au Nanoparticles with Citric Acid as Reductant and Surface Stabilizing Reagent. RSC Adv. 2017, 7, 6187-6192.
-

- 14. Verkhovskii, R.; Kozlova, A.; Atkin, V.; Kamyshinsky, R.; Shulgina, T.; Nechaeva, O. Physical Properties and Cytotoxicity of Silver Nanoparticles under Different Polymeric Stabilizers. Heliyon 2019, 5, e01305.
-

- 15. Choi, J.; Kim, B. H. Ligands of Nanoparticles and their Influence on the Morphologies of Nanoparticle-based Films. Nanomaterials 2024, 14, 1685.
-

- 16. El-Batal, A. I.; Mosalam, F. M.; Ghorab, M. M.; Hanora, A.; Elbarbary, A. M. Antimicrobial, Antioxidant and Anticancer Activities of Zinc Nanoparticles Prepared by Natural Polysaccharides and Gamma Radiation. Int. J. Biol. Macromol. 2018, 107, 2298-2311.
-

- 17. Imanishi, A.; Gonsui, S.; Tsuda, T.; Kuwabata, S.; Fukui, K. I. Size and Shape of Au Nanoparticles Formed in Ionic Liquids by Electron Beam Irradiation. Phys. Chem. Chem. Phys. 2011, 13, 14823-14830.
-

- 18. Naghavi, K.; Saion, E.; Rezaee, K.; Yunus, W. M. M. Influence of Dose on Particle Size of Colloidal Silver Nanoparticles Synthesized by Gamma Radiation. Radiat. Phys. Chem. 2010, 79, 1203-1208.
-

- 19. Afify, T. A.; Saleh, H. H.; Ali, Z. I. Structural and Morphological Study of Gamma‐irradiation Synthesized Silver Nanoparticles. Polym. Compos. 2017, 38, 2687-2694.
-

- 20. Vo, K. D. N.; Kowandy, C.; Dupont, L.; Coqueret, X.; Hien, N. Q. Radiation Synthesis of Chitosan Stabilized Gold Nanoparticles Comparison between E−Beam and γ Irradiation. Radiat. Phys. Chem. 2014, 94, 84-87.
-

- 21. Chappuis, F.; Grilj, V.; Tran, H. N.; Zein, S. A.; Bochud, F.; Bailat, C.; Incerti, S.; Desorgher, L. Modeling of Scavenging Systems in Water Radiolysis with Geant4-DNA. Phys. Med. 2023, 108, 102549.
-

- 22. Plante, I.; Devroye, Considerations for the Independent Reaction Times and Step-by-step Methods for Radiation Chemistry Simulations. Radiat. Phys. Chem. 2017, 139, 157-172.
-

- 23. Baldacchino, G.; Brum, E.; Denden I.; Bouhadoun S.; Roux R.; Khodija H.; Sicard-Roselli C. Importance of Radiolytic Reactions During High‑LET Irradiation Modalities: LET Effect, Role of O2 and Radiosensitization by Nanoparticles. Cancer Nanotechol. 2019, 10, 3.
-

- 24. Chappuis, F. E. Novel Approach to Radiotherapy using Ultra-High Dose Rate Radiations: Uncover the Early Mechanisms of the FLASH Effect with Monte Carlo Techniques. PhD Thesis. Université de Lausanne, Faculté de biologie et médecine, 2023; pp 134.
- 25. Madden, K. P.; Mezyk, S. P. Critical Review of Aqueous Solution Reaction Rate Constants for Hydrogen Atoms J. Phys. Chem. Ref. Data 2011, 40, 023103.
-

- 26. Panariello, L.; Damilos, S.; du Toit, H.; Wu, G.; Radhakrishnan, A. N. P.; Parkin, I. P.; Gavriilidis, A. Highly Reproducible, High-Yield Flow Synthesis of Gold Nanoparticles Based on a Rational Reactor Design Exploiting the Reduction of Passivated Au(III). React. Chem. Eng. 2020, 5, 663-676.
-

- 27. Bui, A.; Bekerat, H.; Childress, L.; Sankey, J.; Seuntjens, J.; Enger, S. A. Effects of Incoming Particle Energy and Cluster Size on the G-Value of Hydrated Electrons. Phys. Med. 2023, 107, 102540.
-

- 28. Korpanty, J.; Parent, L. R.; Gianneschi, N. C. Enhancing and Mitigating Radiolytic Damage to Soft Matter in Aqueous Phase Liquid-Cell Transmission Electron Microscopy in the Presence of Gold Nanoparticle Sensitizers or Isopropanol Scavengers. Nano Lett. 2021, 21, 1141-1149.
-

- 29. Möller, S.; Höschen, D.; Arnoldbik, W.; Tyburska-Pueschel, B. An MeV Proton Irradiation Facility: DICE. Materials 2024, 17, 3646.
-

- 30. Gracien, E. B.; Jérémie, M. L.; Joseph, L. K. K.; Omer, M. M.; Antoine, M. K.; Hercule, K. M.; Gerard, M. N. Role of Hydroxyl Radical Scavenger Agents in Preparing Silver Nanoparticles Under γ-Irradiation. SN Appl. Sci. 2019, 1, 961.
-

- 31. Gachard, E.; Remita, H.; Khatouri, J.; Keita, B.; Nadjo, L.; Belloni, A. J. Radiation-Induced and Chemical Formation of Gold Clusters. New J. Chem. 1998, 22, 1257-1265.
-

- 32. Zharikov, A. A.; Vinogradov, R. A.; Zezina, E. A.; Pozdnyakov, A. S.; Feldman, V. I.; Vasiliev, A. L.; Zezin, A. A. The Radiation-Induced Preparation of Ultrasmall Gold Nanoparticles in Au(III) Complexes with Units of Poly(1-Vinyl-1,2,4-Triazole) and Poly(1-Vinyl-1,2,4-Triazole)-Poly(Acrylic Acid). Colloids Interface Sci. Commun. 2022, 47, 100602.
-

- 33. Kim, E. J.; Yeum, J. H.; Choi, J. H. Effects of Polymeric Stabilizers on the Synthesis of Gold Nanoparticles. J. Mater. Sci. Technol. 2014, 30, 107-111.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2024 Impact Factor : 0.6
- Indexed in SCIE
 This Article
This Article
-
2025; 49(5): 618-625
Published online Sep 25, 2025
- 10.7317/pk.2025.49.5.618
- Received on Mar 25, 2025
- Revised on Apr 28, 2025
- Accepted on May 27, 2025
 Services
Services
Shared
 Correspondence to
Correspondence to
- Chan-Hee Jung
-
Advanced Radiation Technology Institute, Korea Atomic Energy Research Institute, Jeongeup, Jeollabuk-do 56212, Korea
- E-mail: jch@kaeri.re.kr
- ORCID:
0000-0001-7482-9426








 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.