- Effect of Acryl-modified Poly(BA-co-GMA) on Physical Properties of Photo-curable Resin
Department of Polymer Science and Engineering, Sungkyunkwan University, 2066, Seobu-Ro, Jangan-Gu, Suwon-Si, Gyeonggi-Do 16419, Korea
- 아크릴 변성 부틸아크릴레이트 올리고머가 광경화 수지 물성에 미치는 영향
성균관대학교 고분자공학과
Reproduction, stored in a retrieval system, or transmitted in any form of any part of this publication is permitted only by written permission from the Polymer Society of Korea.
The purpose of this study is to investigate acrylic oligomer with excellent flexibility which can be used as a photocurable crosslinking agent. In this study, the acrylate oligomer with the epoxy group was synthesized by free radical polymerization of butyl acrylate (BA) and glycidyl methacrylate (GMA) as reactants. Also, the acryl-modified oligomer with hydroxyl group was synthesized by the reaction of acrylic acid with the epoxy-containing oligomer. Various acryl-modified acrylate oligomers were prepared by changing the concentration of GMA and employing different acrylate monomers such as hexyl acrylate and octyl acrylate with different chain lengths. Photo-cured films were prepared from the synthesized acryl-modified oligomers, reactive diluents, and photoinitiator. And the corresponding curing degree, thermal properties and mechanical properties of the cured film were investigated.
본 연구는 낮은 점도와 우수한 유연성을 바탕으로 광경화 가교제로 사용이 가능한 광경화 올리고머의 합성에 대한 연구이다. 라디칼 중합을 통해 butyl acrylate(BA)와 glycidyl methacrylate(GMA)로부터 에폭시기를 가지는 아크릴레이트 올리고머를 합성한 후, acrylic acid(AA)와 아크릴화 반응을 통해 수산기를 포함하고 있는 아크릴 변성 부틸아크릴레이트 올리고머를 합성하였다. 올리고머의 GMA의 조성, 고분자 주쇄로 사용된 다양한 단량체의 사슬 길이를 변수로 선정하여 5종의 신규 아크릴 변성 올리고머를 제조하였다. 합성한 올리고머를 광개시제 및 다양한 아크릴 단량체와 섞어 광경화형 레진을 배합 후 UV를 조사하여 광경화 필름 시편을 제작하고 gel content, 열 및 기계적 특성을 분석하였다.
In this study, the acryl-modified oligomers with excellent flexibility were synthesized based on poly(butyl acrylate-co-glycidyl methacrylate) and acrylic acid. The newly synthesized oligomers were employed to make various photo-curable acryl samples.
Keywords: photo-curable resin, acryl-modified oligomer, crosslinking agent, butyl acrylate, glycidyl methacrylate.
저자들은 이해상충이 없음을 선언합니다.
광경화는 파장의 길이에 따라 자외선(UV) 경화와 전자선(EB) 경화로 나눠지고 그중 자외선 경화의 사용량이 전 세계 광경화 시장의 90% 이상을 차지하고 있다. 2004년의 미국 UV/EB 경화 국제회의에서 광경화를 efficient(효율적), enabling(다분야 이용 가능), economical(경제적), energy saving(에너지 절감), environmental friendly(친환경적)의 “5E” 특징을 가지고 있는 기술로 정의하였다. UV 경화의 원리는 액체 상태의 광경화 수지가 자외선에 의한 가교 반응을 통해 특정한 물성을 갖춘 고분자로 경화되는 것이다.1-3 1960년 독일 Bayer사가 최초의 자외선 광경화 도료를 개발한 후, UV 경화 제품의 생산량은 매년 12-15%의 증가 속도를 유지하고 있으며 친환경성 및 에너지 절약의 강점을 바탕으로 각 분야에서 빠르게 발전하고 있다. 현재의 광경화 기술은 도료, 잉크, 접착제 같은 전통적인 분야뿐만 아니라 3D 프린팅, 바이오 의료 재료, 전자 재료 그리고 복합 재료 등 새로운 분야에도 응용되고 있다.3,4
광경화 수지는 주로 올리고머, 단량체, 광개시제 및 첨가제로 구성되어 있다. 광경화 단량체는 광경화 속도 및 가교밀도 향상에 우수한 효과가 있으며, 광경화 올리고머는 최종 경화물의 유연성 및 내충격성을 비롯한 기계적 성질에 큰 영향을 미친다. 대표적인 광경화 올리고머로는 우레탄 아크릴레이트와 에폭시 아크릴레이트가 있다.5,6 우레탄 아크릴레이트는 내열성, 유연성 및 내충격성이 우수하지만 점도가 높고 가격이 비싸다는 단점이 있다. 한편, 에폭시 아크릴레이트는 접착력과 경도는 높고 가격이 저렴하여 현재 다양한 분야에 적용되고 있지만 출력물의 유연성이 필요한 3D 프린팅, 광경화 필름과 같은 분야에서는 선호도가 떨어진다. 이는 광경화에 사용되는 대부분의 에폭시 아크릴레이트가 novolac계 에폭시 아크릴레이트와 bisphenol A계 에폭시 아크릴레이트로 분자 구조 내에 빛을 흡수하는 benzene 구조의 특성으로 인해 내부 경화가 부족하기 때문으로 분석된다.1-5,7 또한, 고점도 및 취성이 높은 문제도 있어 과량의 반응성 희석제(단량체)가 필요하다는 단점 역시 지적된다.8,9 경화도 부족의 문제를 해결하기 위해 사용되는 가장 보편적인 방법은 광경화성 가교제를 함께 사용하는 방법이 있다. 여기에 사용되는 대표적인 광경화성 가교제로는 다관능성의 특성을 가지는 pentaerythritol tetraacrylate(PETTA)와 dipentaerythritol hexaacrylate(DPHA)가 있다.4,5 이러한 가교제는 경화 제품의 경화 속도, 가교 밀도를 증가시킴으로써 경화도를 보완하고 이를 통해 경도 등의 물성을 증가시키지만 여전히 점도와 취성의 문제가 남아있다.4-9
본 연구에서는 benzene 구조가 없는 에폭시 아크릴레이트 단량체(glycidyl methacrylate)를 이용하여 광경화 가교제로 적용할 수 있으며 점도가 낮고 유연성이 우수한 아크릴 변성 에폭시 올리고머의 합성을 목표로 한다. Butyl acrylate(BA) 고분자는 유리 전이 온도가 낮고 내구성이 높을 뿐만 아니라 단량체의 가격도 저렴하기 때문에 주로 soft segment로 고분자 중합에 사용되어왔다.10-20 따라서 본 연구에서는 BA를 고분자 주쇄의 기반으로 하고, glycidyl methacrylate(GMA)와 acrylic acid(AA)를 반응하여 다양한 아크릴 변성 poly(BA-co-GMA)를 합성하였다. 또한 사슬 조성이 광경화 수지의 물성에 어떤 영향을 미칠 수 있는지를 관찰하기 위해 hexyl acrylate와 octyl acrylate를 사용하여 아크릴 변성 poly(HA-co-GMA)와 아크릴 변성 poly(OA-co-GMA)를 각각 합성하여 비교하였다. 한편, 가교제로 가장 보편적으로 사용되는 DPHA와의 비교를 통해 합성된 올리고머의 가교제 역할 및 광경화 수지의 물성에 어떤 영향을 미치는지에 대해 조사하였다.
시약 및 재료.아크릴 변성 부틸 아크릴레이트 올리고머를 합성하기 위하여 butyl acrylate(BA), acrylic acid(AA), benzyl triethyl ammonium bromide는 Sigma-Aldrich사(미국), hexyl acrylate(HA)와 octyl acrylate(OA)는 TCI사(일본), glycidyl methacrylate(GMA), 2,2-azobisisobutyronitrile(AIBN), 1-dodecanethiol, toluene, butyl acetate, sodium carbonate는 Samchun Chemical(한국)에서 구매하여 별도의 정제 과정없이 사용하였다.
광경화 필름을 제작하기 위해 Miwon Specialty Chemical 사(한국)의 hexanediol diacrylate(HDDA)와 tripropylene glycol diacrylate(TPGDA)를 사용하였고, 2,4,6-trimethylbenzoyl di- phenylphosphine oxide(TPO)는 IGM Resin(미국)사에서 구매하여 사용하였다.
에폭시 함유 아크릴레이트 올리고머 합성. 환류 냉각기와 온도계, 그리고 교반기를 갖춘 250 mL의 3-neck round bottom flask에 반응물 BA와 GMA를 각각 95:5, 90:10, 85:15의 몰 비율로 투입하고 개시제 AIBN(2.5 wt% of monomer), chain transfer agent인 1-dodecanethiol(10-14 mol% of monomer) 그리고 반응 용매로 toluene(30 wt% solid contents)을 각각 투입하였다. 반응기에 있는 산소를 제거하기 위해 질소를 주입하며 상온에서 magnetic stirrer를 이용하여 700 rpm의 속도로 30분 동안 교반하였다. 이후, 내부 온도를 85 oC까지 승온시키고 5시간 동안 반응을 진행하였다. 한편 알킬 그룹의 길이가 광경화 수지의 물성에 미치는 영향을 확인하기 위해 BA 외에 HA, OA를 각각 사용하여 GMA와 85:15의 몰 비율로 합성하였다(Scheme 1).

Scheme 1. Synthetic scheme of poly(BA-co-GMA), poly(HA-coGMA) and poly(OA-co-GMA).
반응 종료 후, methanol과 deionized water(V/V=9/1)의 혼합 용매를 이용해 잔존 단량체와 개시제를 제거하였고 중합된 올리고머를 침전시켰다. 세척 후, 생성물을 vacuum oven을 이용하여 50 oC에서 24시간 동안 건조하여 5종의 에폭시 함유 아크릴레이트 올리고머를 제조하였다.
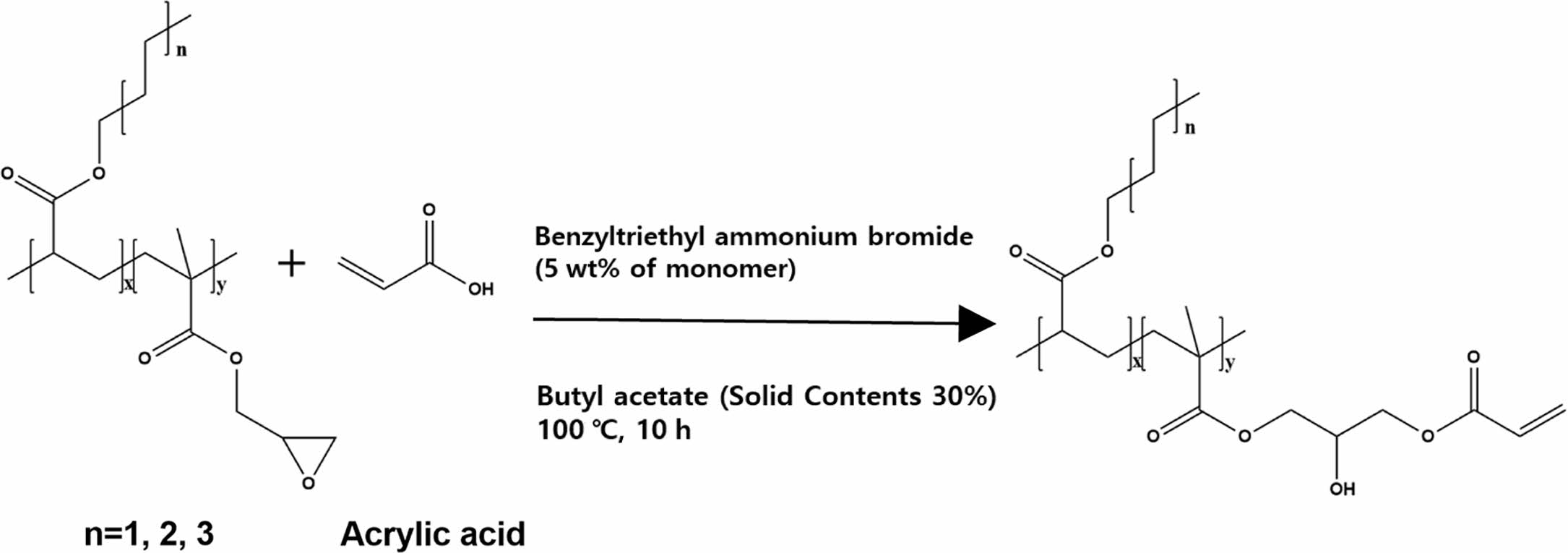
아크릴 변성 에폭시 아크릴레이트 올리고머 합성.환류 냉각기와 온도계 그리고 교반기가 설치된 250 mL의 3-neck round bottom flask에 합성된 에폭시 함유 아크릴레이트 올리고머를 투입하고 AA(1.5 molar ratio), 촉매 benzyltriethyl ammonium bromide(5 wt% of monomer), 용매 BA(30 wt% solid contents)를 투입하였다. 반응기를 질소 분위기하에서 magnetic stirrer를 이용하여 700 rpm의 속도로 교반하며 내부 온도를 100 oC로 유지, 10시간 동안 반응을 진행하였다(Scheme 2). 반응 종결 후, 잔존 AA와 촉매 benzyltriethyl ammonium bromide를 제거하기 위해 10% sodium carbonate 수용액을 제조, separating funnel을 이용하여 분리정제를 진행하였다. 이후 deionized water(DIW)를 이용한 추가적인 세척을 진행하였고 남아있는 용매를 rotary evaporator와 vacuum oven를 이용하여 제거하였다. 획득한 올리고머는 BA와 GMA의 비율에 따라 BA95/5, 90/10, 85/15로 명명하였고, HA를 acrylic backbone으로 합성한 올리고머는 HA85/15, OA를 acrylic backbone으로 합성한 올리고머는 OA85/15로 각각 명명하였다.
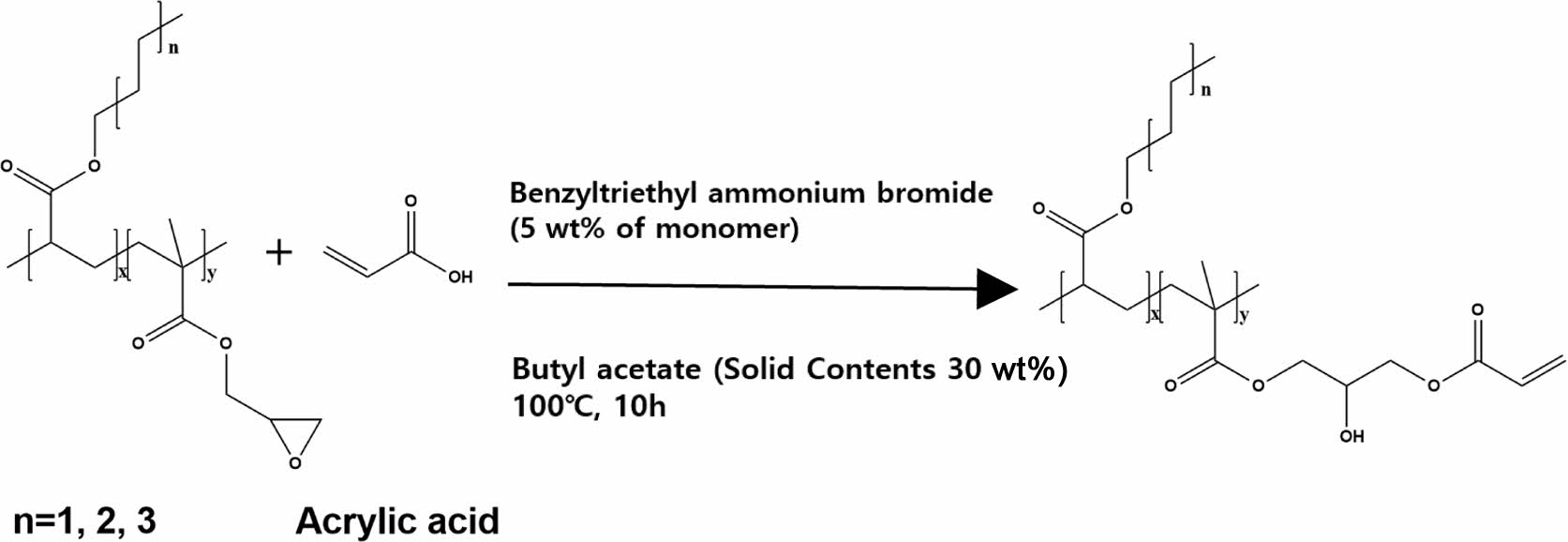
Scheme 2. Synthetic scheme of acryl-modified acrylate oligomers.
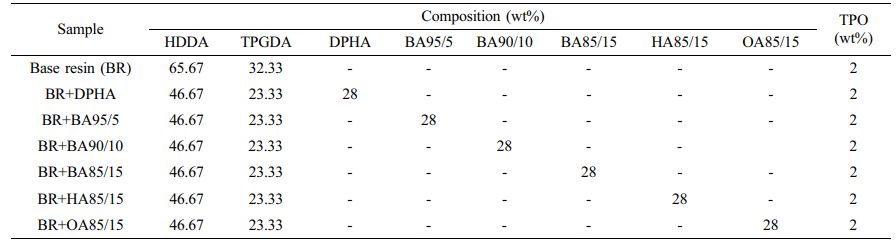
광경화 필름 시편 제작.광경화 필름을 제작하기 위하여 hexanediol diacrylate(HDDA)와 tripropylene glycol diacrylate (TPGDA)를 2:1의 무게 비율로 base resin(BR)을 제조하였다. Table 1의 배합비에 따라 UV가 차단되어 있는 vial에 BR 70 g, 합성된 아크릴 변성 올리고머 28 g, 광개시제 TPO 2 g을 투입하고 magnetic stirrer를 이용하여 600 rpm으로 30분간 교반하였다. 제작된 광경화 수지를 10×10 cm 유리판에 두께가 250 mm가 되도록 film applicator로 코팅한 후, 600W 고압 수은 UV 램프를 이용하여 60초간 광경화를 진행하였다. 광경화 후, 경화 필름 시편을 유리판에서 분리, 물성 평가를 진행하였다.
화학 구조 및 분자량 분석.합성한 아크릴 변성 올리고머의 화학구조는 FTIR과 1H NMR을 통해 분석하였다. FTIR 스펙트럼은 Thermal Fisher Scientific 사(미국)의 Nicolet iS5 모델을 이용하여 4000-500 cm-1에 해당하는 파장 영역을 분석하였다. 1H NMR 스펙트럼은 Varian Technology사(미국)의 Unity Inova 모델을 이용하였고 시료는 deutero-chloroform (CDCl3)로 용해한 후 분석하였다. 분자량 측정은 GPC(미국, Agilent사의 1100S 모델)를 이용하여 분석하였다.
점도 분석. 합성한 아크릴 변성 올리고머의 점도를 분석하기 위하여 Brookfield 사(미국)의 LV-DVE모델의 Rotational Viscometer를 사용하였다. 분석은 25 oC 조건에서 Spindle#62를 사용하여 토크를 70-80%로 유지하며 분석하였다.
Gel Content 측정.UV 경화 시간에 따른 광경화 필름의 경화도를 비교하기 위해, 시간별로 경화 후 필름을 적정 용매에 투입 후 무게의 차이를 이용하여 gel content를 분석하였다. 먼저 전자저울을 이용하여 광경화 필름 시편의 초기 무게 W1를 측정한 후, tetrahydrofuran(THF) 용매에 함침하였다. 24시간 후, 용매에 함침시켰던 필름을 50 oC convection oven에서 건조한 후, 광경화 필름 시편의 무게 W2를 측정하였다. Gel content의 계산식은 다음과 같이 나타내었다.
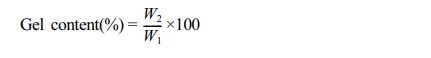
여기서,W1: 광경화 후 필름의 무게, g
W2: 용매에 함침한 후 건조된 필름의 무게, g
열적 특성 평가.제작된 광경화 필름 시편의 열 안정성을 분석하기 위해 TA Instruments사(미국)의 Q50 모델의 TGA를 사용하였다. 분석 조건은 질소 분위기 하에서 30 oC부터 600 oC까지 10 oC/min로 승온시키며 중량 변화에 따른 열분석을 실시하였다. 제작된 광경화 필름의 유리전이온도(Tg)를 확인하기 위해 Seiko Instrument 사(일본)의 Exstar 6000 모델의 DMA를 사용하였다. 분석 조건을 주파수가 1 Hz인 tension mode 에서 0 oC부터 150 oC까지 5 oC/min로 승온하며 진행하였다.
기계적 특성 평가.제작된 광경화 필름의 인장강도, 연신율, 모듈러스를 측정하기 위해 LLOYD Instruments사(미국)의 LR30K plus 모델(Load cell 규격 250N)의 UTM를 사용하였다. 시편의 사이즈는 50×20 mm로 제작하였고 인장 속도는 50 mm/min로 측정하였다. 경도 측정은 Asker사(미국)의 Shore Durometer(A type)를 사용하였다. 측정 조건은 ASTM D2240에 준하여 광경화 시편을 제작 후, 시편에 기계의 Indenter로 완전히 찌른 후 5초 후의 데이터를 측정하였다. 분석은 5회를 측정하여 최대값과 최소값을 제외한 데이터의 평균값으로 계산하였다.
|
Table 1 Composition of Photo-curable Resin Containing Synthesized Acrylic Oligomer and DPHA |
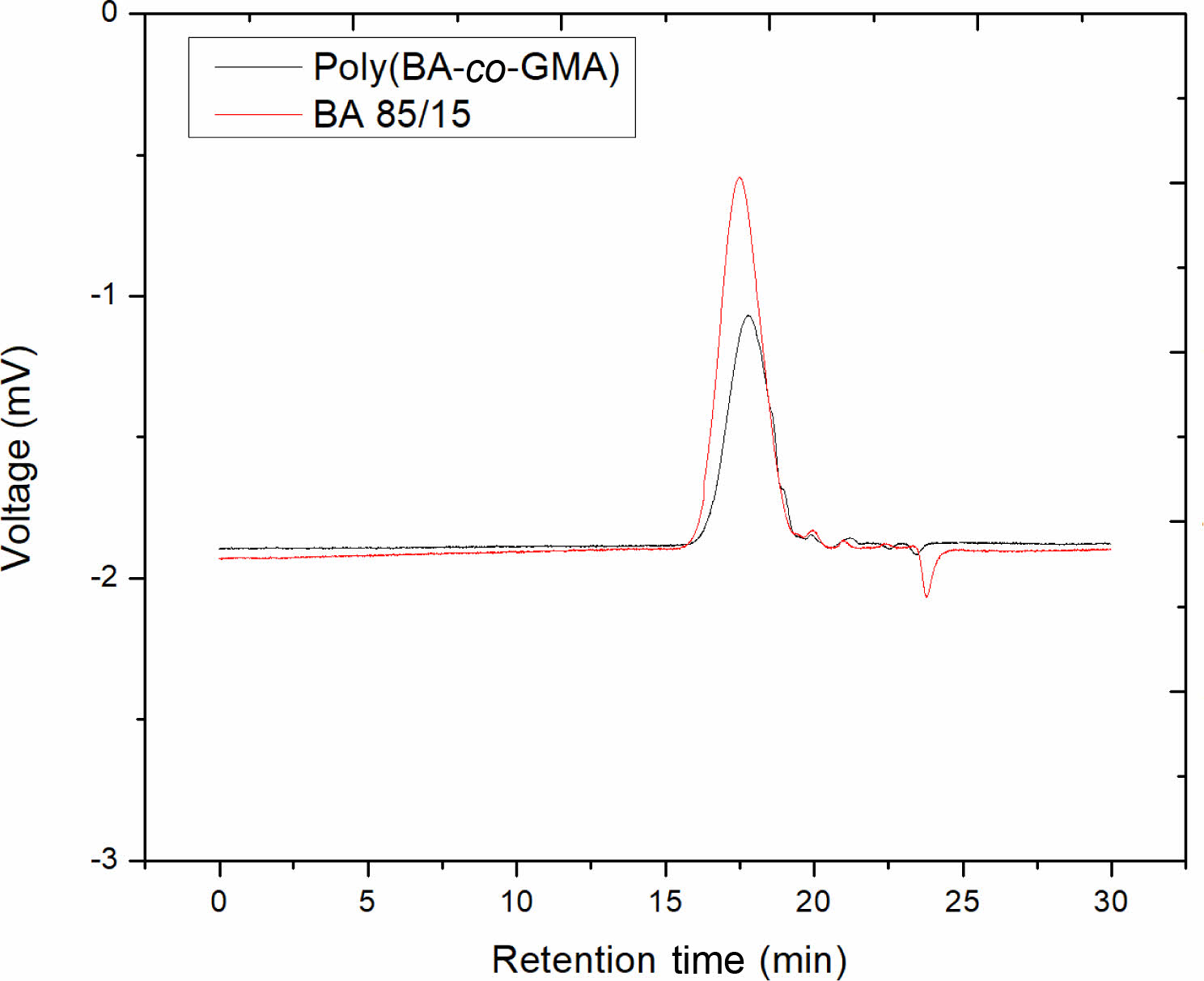
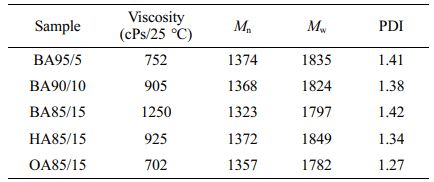
아크릴 변성 아크릴레이트 올리고머 합성. 본 연구에서는free-radical polymerization을 통해 GMA와 사슬 길이가 다른 3종의 아크릴계 단량체(BA, HA 및 OA)를 이용하여 다양한 올리고머를 합성한 후, 합성된 올리고머를 AA와 반응시켜 목표 분자량 1300-1400의 5종의 신규 아크릴 변성 아크릴레이트 올리고머를 합성하였다. 합성한 5종의 신규 아크릴레이트 올리고머의 점도, 분자량, polydispersity index(PDI)를 Table 2에 정리하였다. 합성한 올리고머의 점도는 비교 대상으로 선정한 대표적인 광경화 가교제 DPHA의 1/4 정도인 702-1250 cPs로 나타났다. Figure 1에 나타난 바와 같이 아크릴화 반응에서 AA 투입 후, 반응에 의해서 올리고머의 분자량은 1280에서 1323으로 소폭 증가하는 것이 관찰되었고, 조건을 달리 합성한 5종의 아크릴 역시 비슷한 분자량으로 합성된 것이 관찰되어 중합 및 후속적인 아크릴 변성이 이루어진 것을 확인하였다.
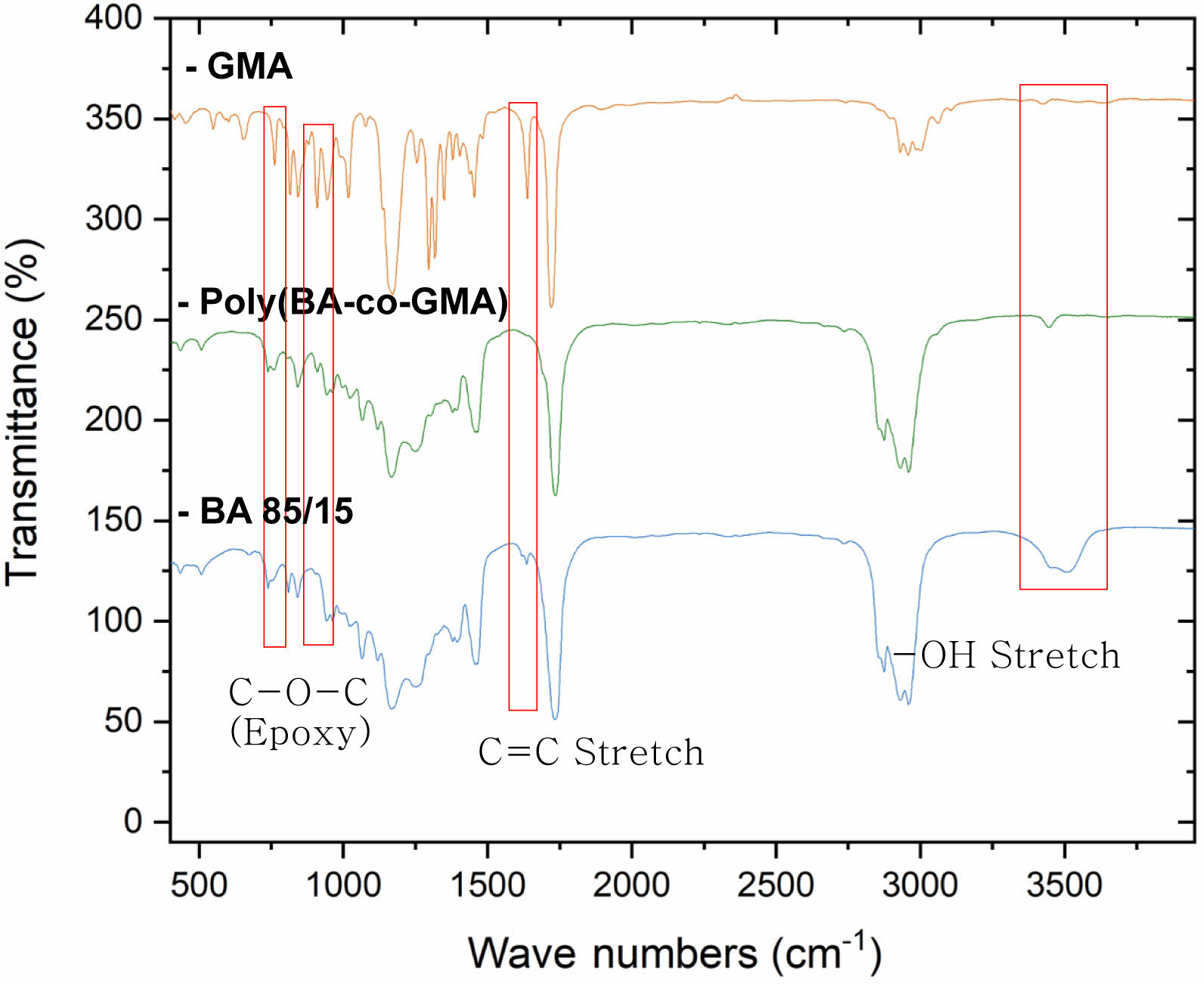
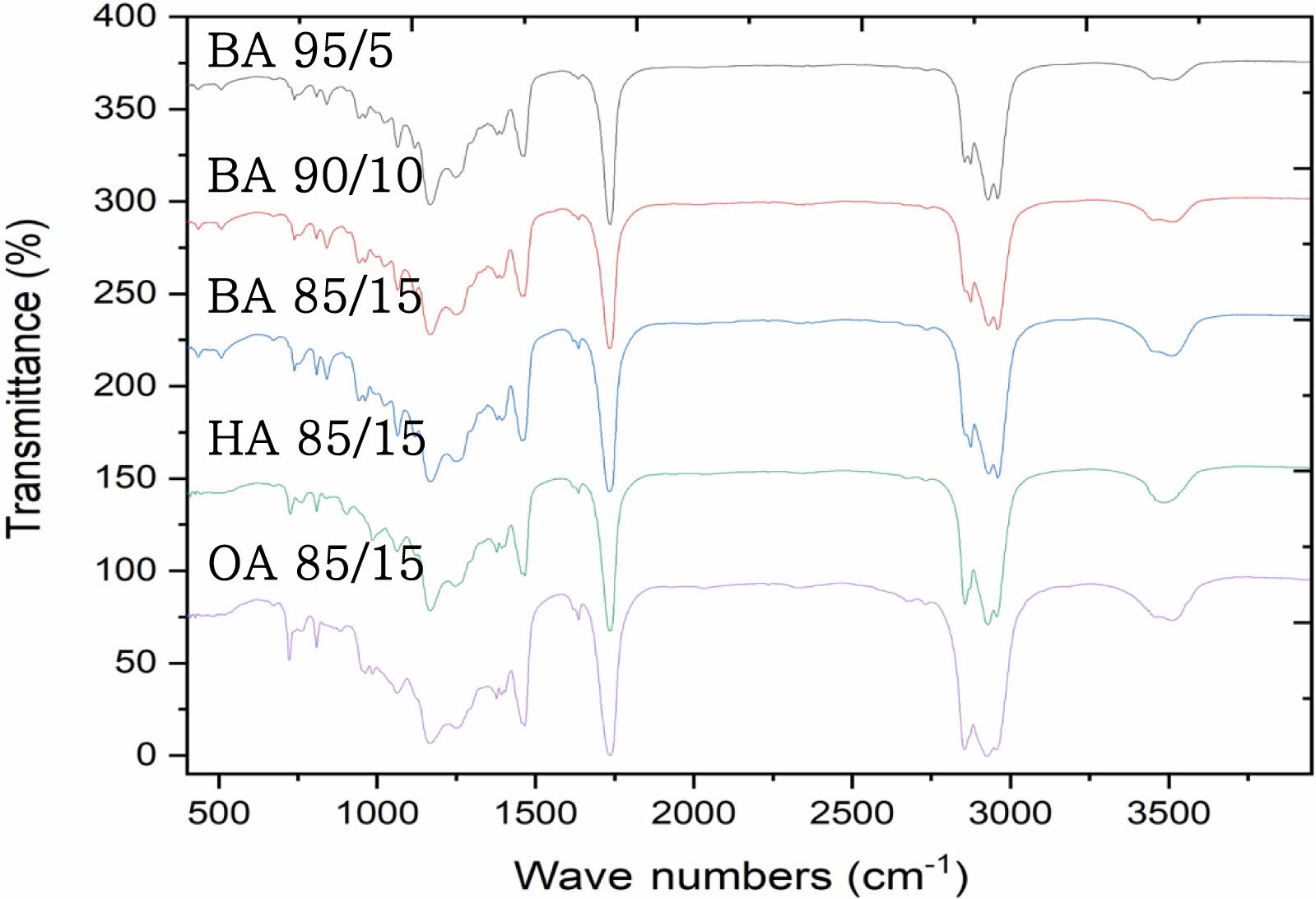
Figure 2에서 glycidyl methacrylate의 에폭시기(C-O-C)는 760 및 909 cm-1에서 피크가 관찰되었다. 한편, 아크릴 변성 Poly(BA-co-GMA)의 FTIR 스펙트럼에서는 에폭시에 해당하는 피크가 완전히 사라졌고 아크릴 변성에 따른 수산기(-OH)피크가 3600-3300 cm-1의 영역에서 관찰되었다. 1700-1550 cm-1 영역에서는 BA85/15 올리고머의 아크릴 관능기로 추정되는 피크가 관찰되었다. 한편, Figure 3을 통해 올리고머 합성 시 GMA의 비율이 높아짐에 따라 합성된 아크릴 변성 poly(BA-co-GMA)의 C=C 결합(1700-1550 cm-1)과 수산기(3600-3300 cm-1)의 피크가 커지는 것을 확인하였다.
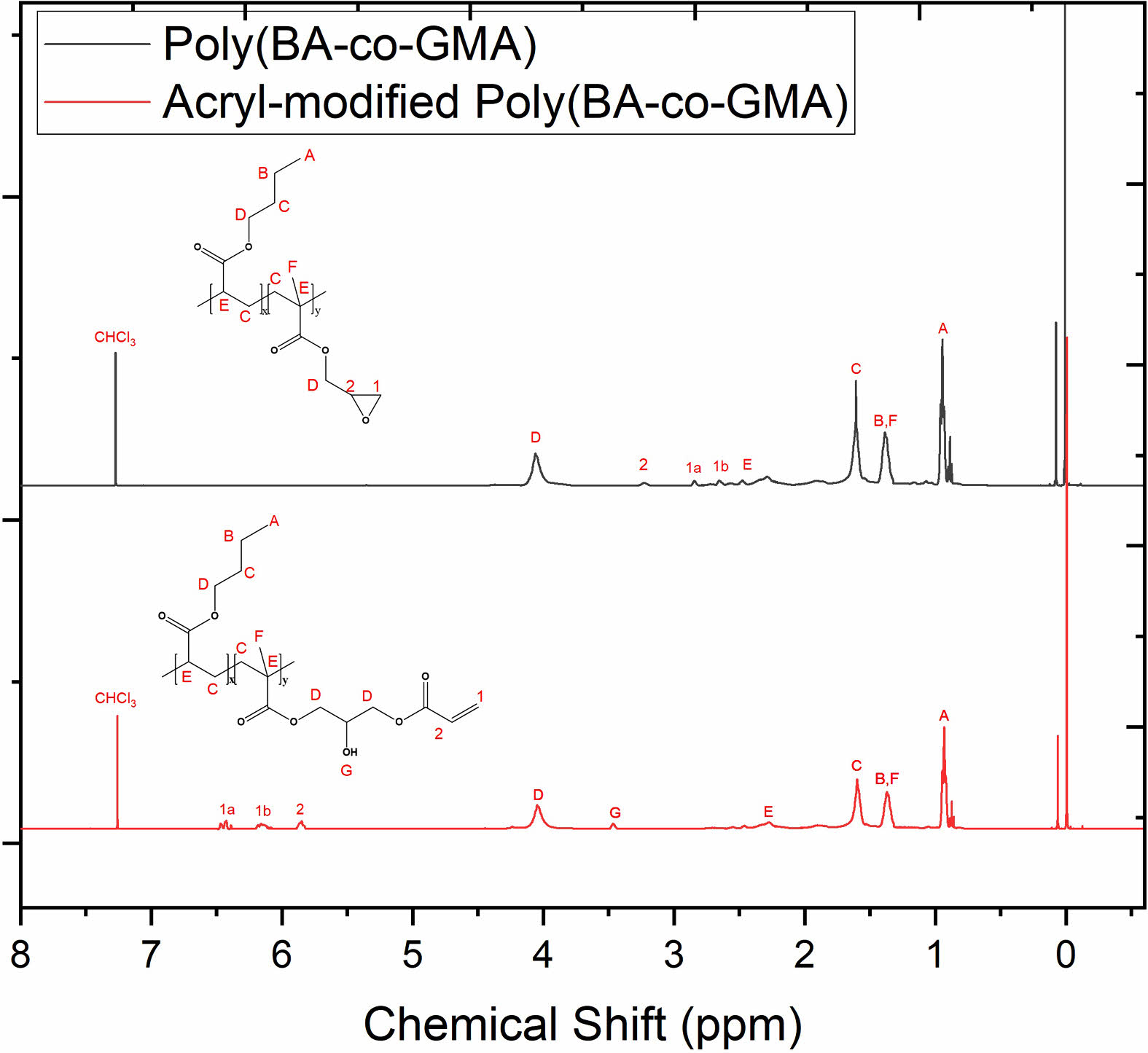
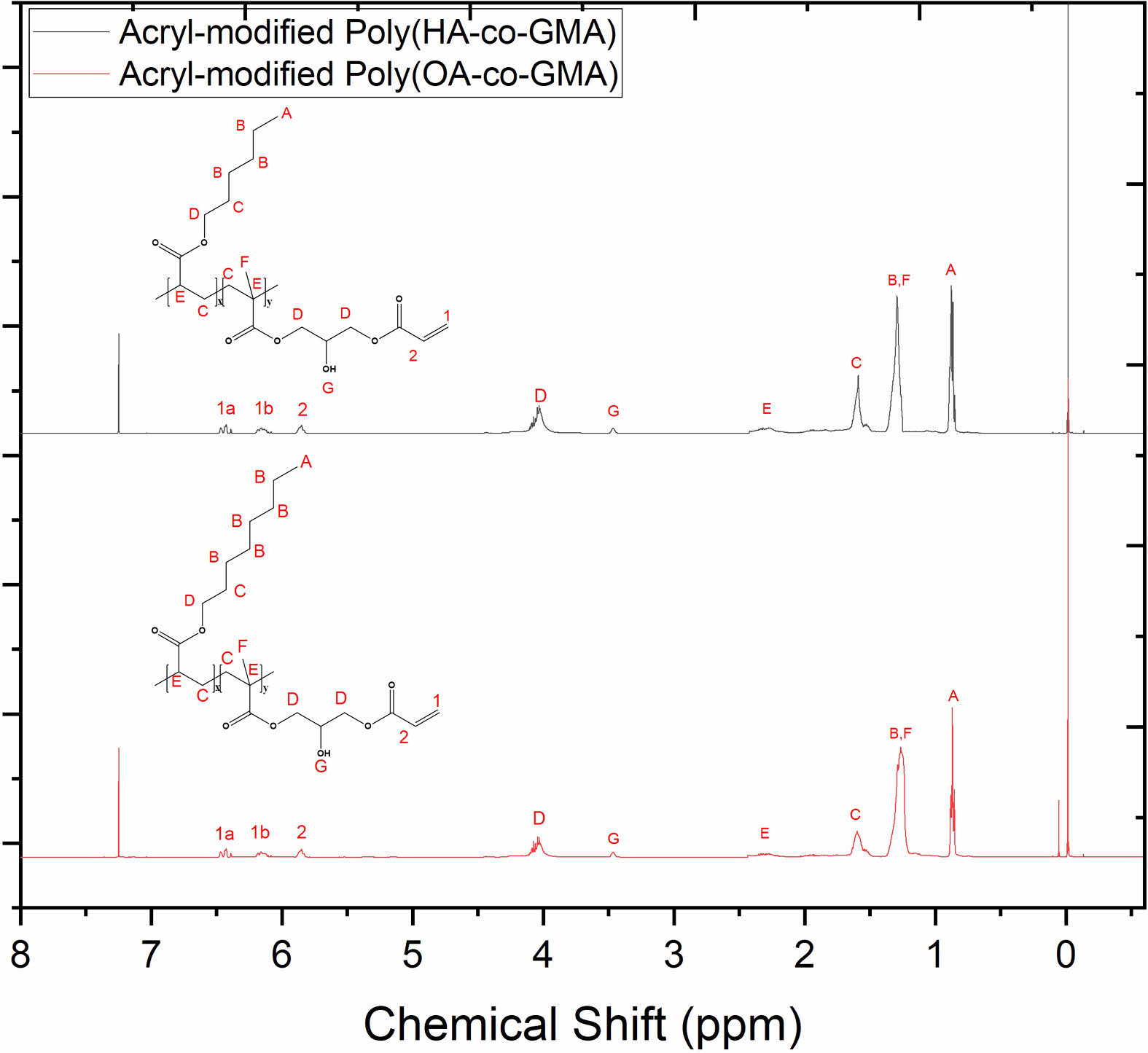
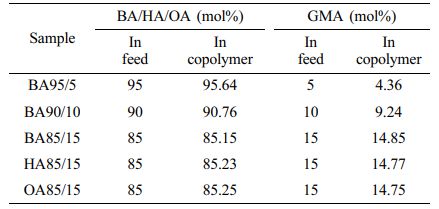
Figure 4와 Figure 5는 합성한 아크릴 변성 아크릴레이트 올리고머의 1H NMR의 스펙트럼이다. Figure 4에서 poly(BA-co-GMA)의 아크릴 변성 전후 1H NMR 스펙트럼 변화를 확인하였다. 아크릴 변성전에는 poly(BA-co-GMA)의 분자 내 에폭시 피크가 2.68, 2.85 및 3.16 ppm에서 관찰되었지만 아크릴 변성 후에는 존재하던 에폭시 피크가 모두 사라졌고 5.78, 6.13 및 6.45 ppm에서 이중결합에 해당하는 피크가 나타났으며, 3.49 ppm에서 수산기 피크가 나타난 것을 추가로 관찰하였다. Table 3은 1H NMR 데이터를 바탕으로 합성한 아크릴 변성 아크릴레이트 올리고머의 조성비를 계산한 결과이다.
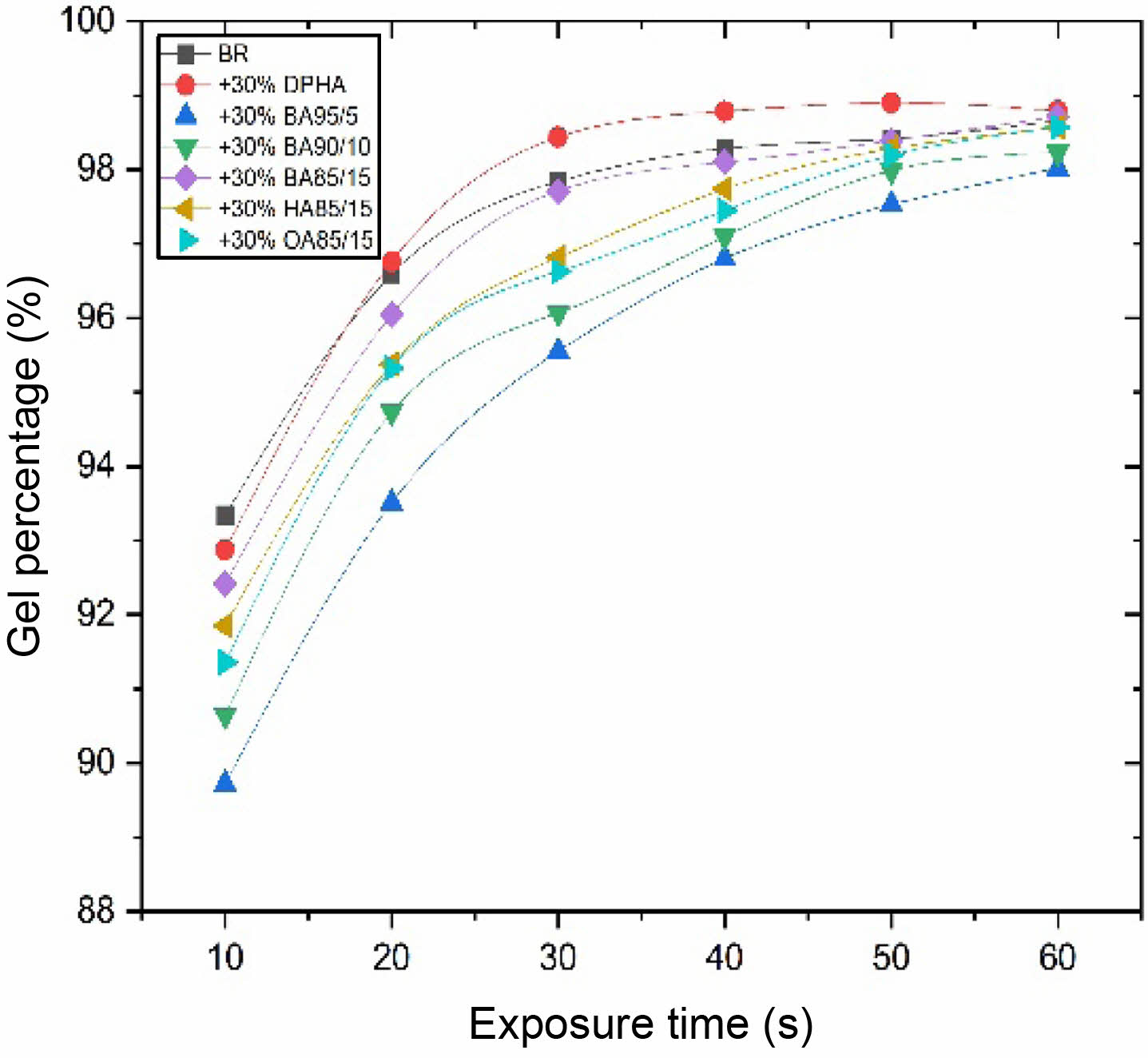
광경화 필름(10×10 cm)시편의 Gel content 측정. 본 광경화 연구에서는 TPO 외에도 기타 acetophenone 및 benzophenone계의 IRGACURE 시리즈의 광개시제가 시도되었지만 TPO가 가장 광경화 효율이 우수하여 이를 기초로 각종 샘플이 제작되었다. UV 조사 시간에 따른 필름의 gel content 함량을 측정하여 Figure 6에 나타내었다. 제작한 광경화 필름 시편은 THF 용매에 함침 후 용출되는 양을 이용하여 gel content를 측정하였다.
노광 시간이 증가함에 따라 TGA상에서는 열분해거동의 변화가 미미하였지만 광경화도가 증가하면 gel content가 증가하는 것을 관찰하였다. 합성한 분자량 1300-1400의 아크릴 변성 올리고머의 경우 DHPA에 비해 사슬 길이가 비교적 길어 초기 경화 속도는 약간 느리지만, 50초 이상 충분히 노광 시 97.53% 이상의 gel content가 나타나는 것을 관찰하였다. 한편, UV 조사 시간이 같을 시 GMA의 함량이 증가할수록 경화도 역시 증가하는 것을 관찰하였다. 이는 GMA의 비율이 증가함에 따라 합성한 올리고머의 광감성 관능기인 이중결합이 증가하기 때문인 것으로 추정된다. 아크릴레이트의 알킬 그룹의 길이 역시 경화도에 영향을 주는 것이 관찰되었는데 알킬 그룹의 길이가 긴 HA와 OA를 사용한 경우 경화 속도 및 경화도(gel content)가 감소하는 것으로 보아 알킬 그룹의 길이가 길어질수록 입체 장해가 증가하여 경화도가 감소하는 것으로 추정된다.
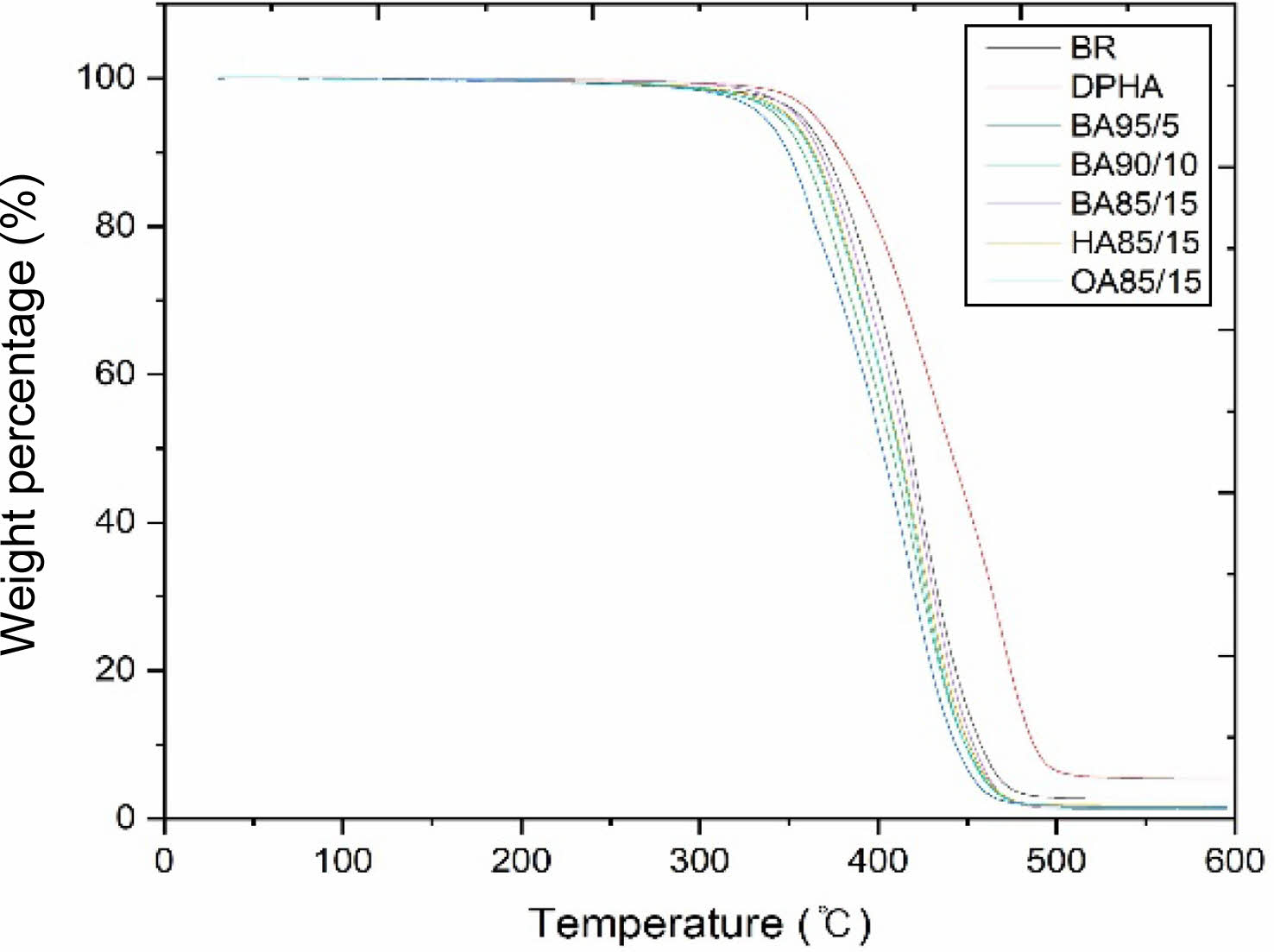
열 특성 평가.광경화 필름 시편의 열분해 거동을 측정한 결과를 Figure 7에 나타내었다. 일반적으로, TGA의 100-300 oC 사이에서는 광개시제, 경화가 안된 저분자량의 올리고머 및 단량체가 열분해된다. Figure 7의 결과를 살펴보면, 300 oC 전에는 무게 변화가 거의 없는 것을 확인할 수 있다. 이를 통해 DPHA 뿐만 아니라 본 연구에서 합성한 아크릴 변성 올리고머를 광경화 가교제로 사용하여 제작된 광경화 필름의 경우 충분한 경화가 이루어진 것으로 판단되었다. 한편, BA 시리즈 올리고머의 경우 아크릴 함량이 늘어날수록 열분해 개시 온도(Td)는 소폭 증가하는 것이 관찰되었다.
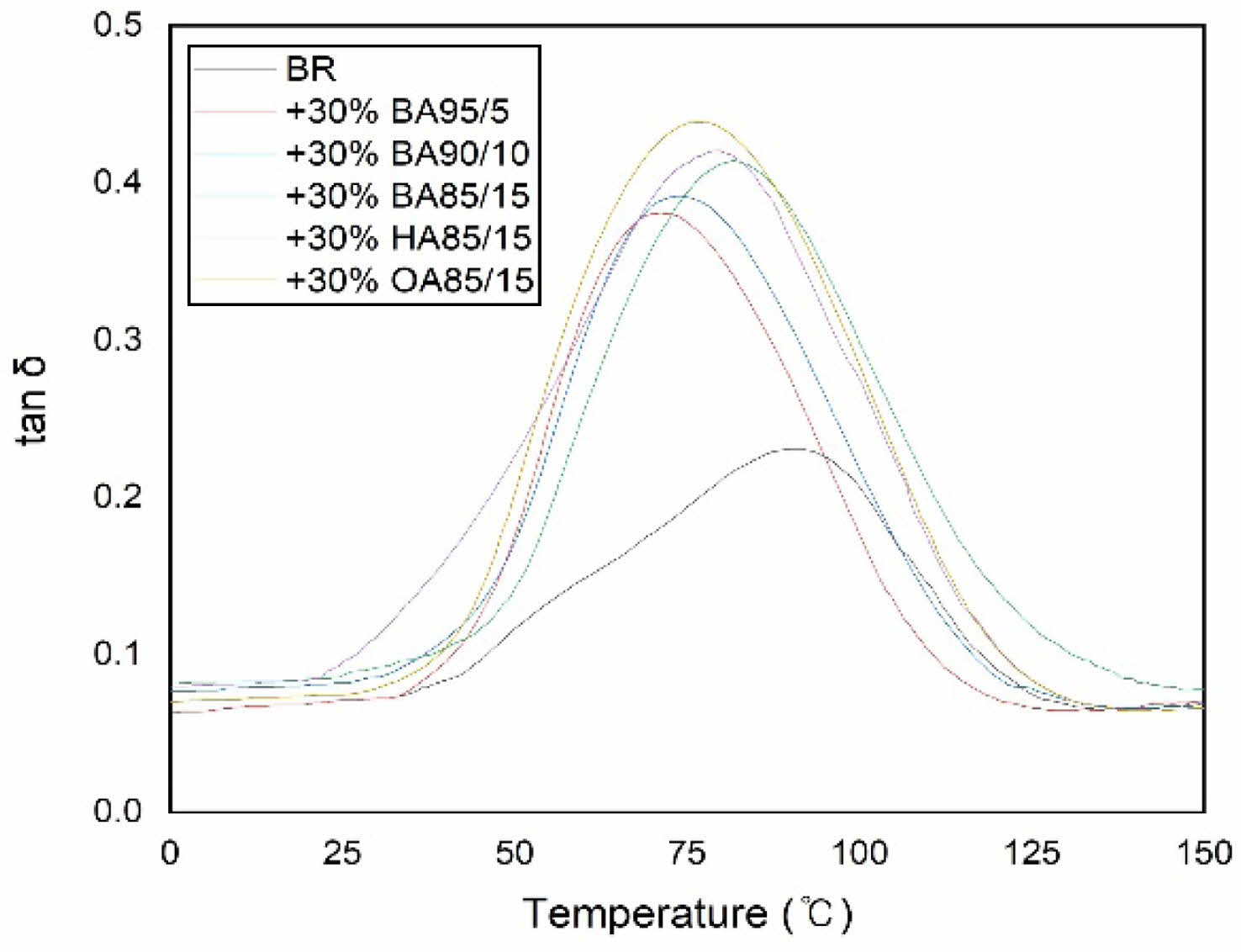
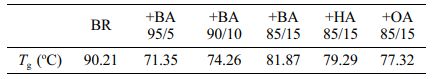
Figure 8은 합성한 아크릴 변성 올리고머로 제작한 필름의 DMA 결과이다. 실험 결과, 합성한 아크릴 변성 올리고머를 광경화 수지에 첨가하여 제작한 시편의 경우 BR만을 사용하여 제작한 시편보다 유리전이온도가 감소되는 것을 확인할 수 있었다. 합성한 아크릴 변성 올리고머의 경우 사용한 아크릴레이트의 알킬 그룹의 길이가 길어질수록 유리전이온도가 낮아지는 것을 관찰할 수 있었다. 이는 합성한 올리고머를 사용할 경우 고분자 사슬 내의 soft segment로 작용할 수 있는 부분이 늘어나 유연성이 증가했기 때문으로 추정된다. 각 샘플의 측정된 Tg의 결과는 Table 4에서 나타내었다. BA 시리즈 올리고머의 경우 아크릴 함량이 늘어날수록 광가교성 관능기의 농도가 증가하게 되어 최종 광경화물의 가교도는 증가하는 효과에 의해서 Tg는 명확하게 증가하는 것이 관찰되었다.
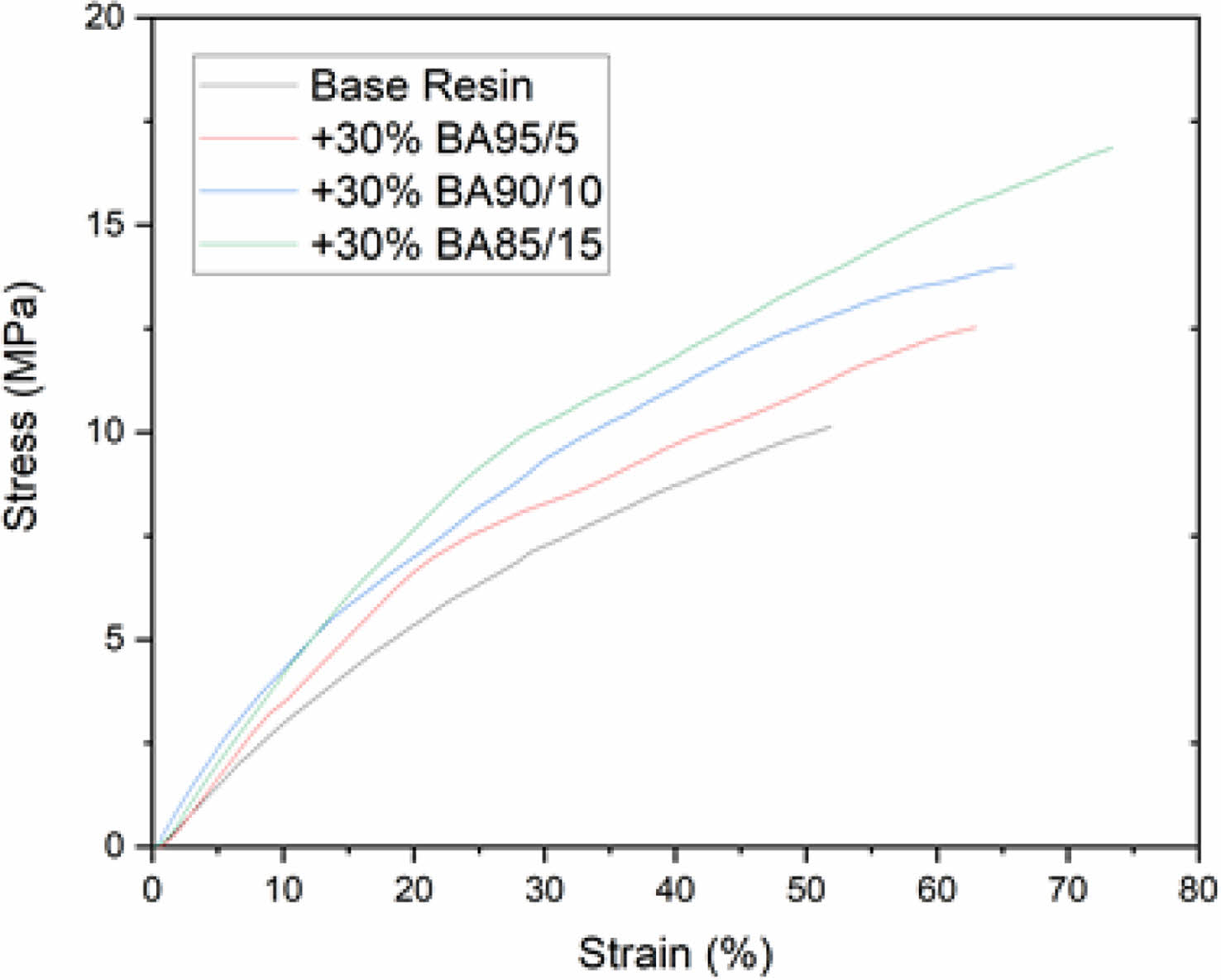
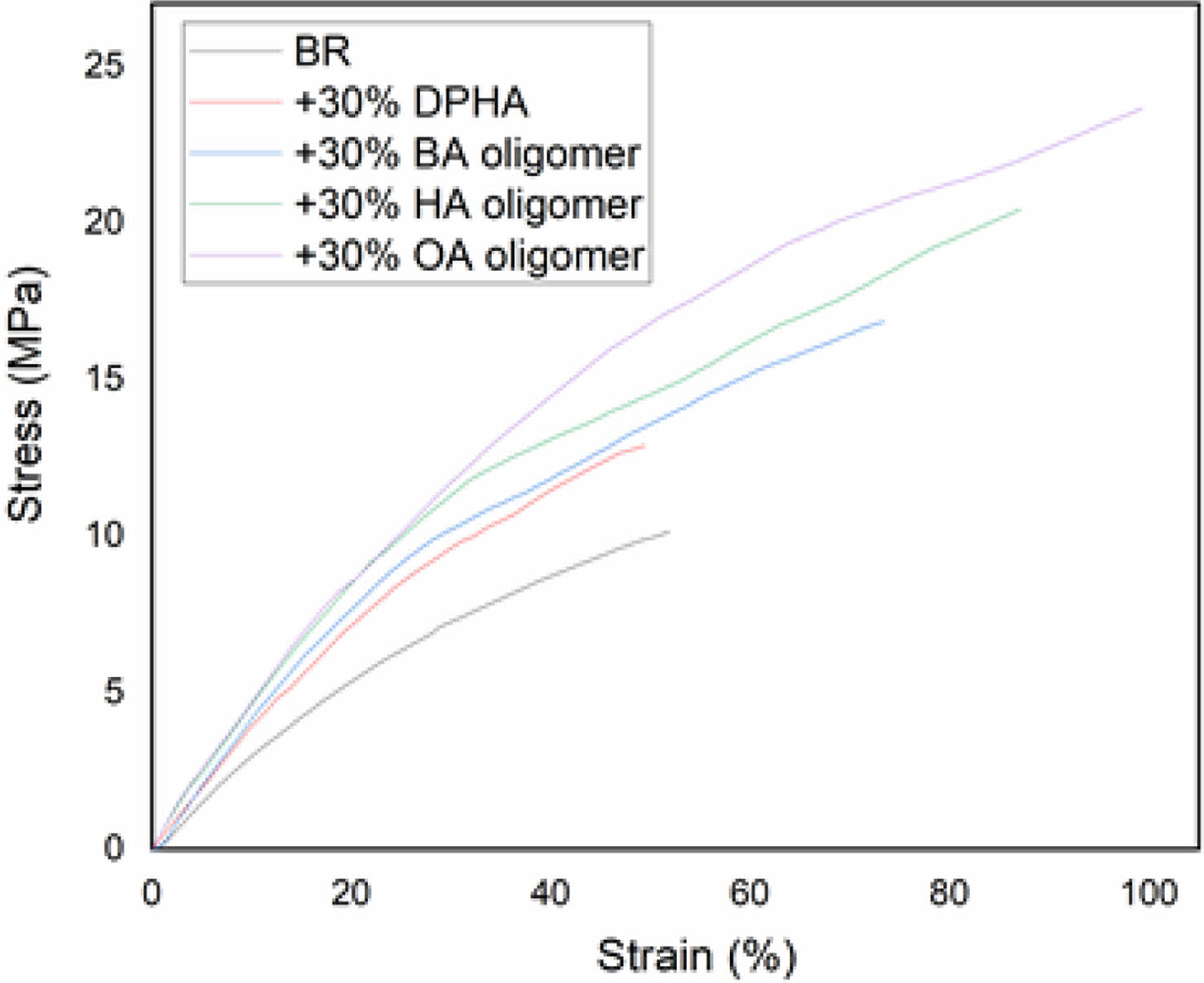
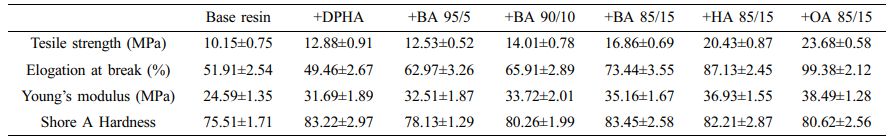
기계적 특성 평가. 본 연구에서 제작한 광경화 필름 시편의 기계적 물성 분석을 위해 UTM을 사용하여 필름의 인장강도(tensile strength), 연신율(elongation at break) 및 modulus를 측정하였다. Figure 9와 Figure 10은 합성한 5종의 아크릴 변성 올리고머가 포함된 수지로 제작한 광경화 시편의 strain-stress curve이며 Table 5는 광경화 시편의 기계적 물성 측정 결과이다. 실험 결과, GMA의 함량이 증가할수록 인장강도, 연신율 및 모듈러스가 증가하는 것이 관찰되었다. 이러한 경향은 이중결합의 비율이 증가하여 가교밀도와 분자량이 증가했기 때문으로 판단된다. 단량체의 알킬 그룹의 길이가 길어질수록 연신율과 인장강도가 증가되는 것도 관찰되었다. 이는 고분자 사슬 내의 soft segment 비율이 증가함에 따라 유연성이 증가했기 때문으로 추정된다.
Figure 10에 의하면 DPHA를 추가하여 사용한 시편의 경우 BR만을 사용하여 제작한 시편보다 인장강도는 2.73% 증가하지만 연신율이 2% 이상 감소하는 것을 관찰할 수 있었다. 이는 DPHA가 6개의 아크릴 관능기를 가지고 있기 때문에 가교 밀도가 증가했기 때문으로 판단된다.
경도 분석은 Shore A durometer를 이용하여 Shore A 경도를 측정하였다. Table 5에 나타난 결과를 통해 합성된 아크릴 변성 올리고머(BA95/5, BA90/10, BA85/15)를 첨가하여 제작된 광경화 시편의 Shore A경도가 2.62-7.94 증가하는 것을 관찰하였다. 한편, 합성한 올리고머에 사용된 단량체의 알킬 그룹의 길이가 길어질수록 경도가 낮아지는 것이 관찰되었다. 이는 분자 구조 내 soft segment의 비율이 증가했기 때문으로 추정된다. 한편, 합성한 올리고머의 GMA 비율이 증가할수록 경도 값이 증가하는 것이 관찰되었는데, 이는 이중결합의 비율이 증가하여 가교 밀도가 증가했기 때문으로 추정된다. 뿐만 아니라 GMA 분자 구조에 메틸기(-CH3)가 있기 때문에 GMA의 함량이 높아질수록 경도가 높아질 수 있는데, 그중 BA85/15로 제작된 경화 필름의 Shore A hardness는 DPHA와 비슷한 수치인 83.45로 가장 높게 나타났다.
|
Figure 1 GPC traces of poly(BA-co-GMA) and its corresponding acryl-modified BA oligomer. |
|
Figure 2 FTIR spectra of GMA, poly(BA-co-GMA) and BA85/15. |
|
Figure 3 FTIR spectra of synthesized acryl-modified oligomers with different GMA contents. |
|
Figure 4 1H NMR spectra of synthesized poly(BA-co-GMA) and acryl-modified poly(BA-co-GMA). |
|
Figure 5 1H NMR spectra of synthesized acryl-modified poly(HAco-GMA) and acryl-modified poly(OA-co-GMA). |
|
Figure 6 The gel percentage of photo-cured films based on synthesized acryl-modified oligomers with different UV exposure time. |
|
Figure 7 The TGA thermograms of photo-cured films which contained various synthesized acryl-modified oligomers under N2 atmosphere. |
|
Figure 8 DMA curves of photo-cured films which contained various synthesized acryl-modified oligomers. |
|
Figure 9 Stress-strain curves of photo-cured films which contained various synthesized BA oligomers. |
|
Figure 10 Stress-strain curves of photo-cured films which contained various synthesized BA85/15, HA85/15, OA85/15, and DPHA. |
|
Table 2 Viscosity, Molecular Weight and PDI Results of Synthesized Acryl-modified Oligomers |
|
Table 4 The Glass Transition Temperature Results of Photocured Films Which Contained Various Synthesized Acrylmodified Oligomers |
|
Table 5 Mechanical Properties of Photo-cured Film Which Contained Synthesized Acryl-modified Oligomers (30 wt%) |
본 연구에서는 알킬 그룹의 길이가 다른 3종의 아크릴레이트 단량체(BA, HA, OA)와 GMA를 이용하여 free-radical polymerization를 통해 GMA 함량이 다른 5종의 에폭시 함유 아크릴레이트 올리고머를 중합하였다. 그 후 중합된 올리고머를 AA와 반응하여 아크릴 변성 아크릴레이트 올리고머를 각각 합성하였고, 기본 광경화 수지와 배합하여 UV 램프를 이용해 광경화 시편을 제작하였다. 이후 gel content를 통한 경화도 측정, 열적 특성 및 기계적 특성을 분석하여 합성한 아크릴 변성 올리고머가 광경화 수지의 물성에 미치는 영향에 대한 연구를 수행하였다.
합성한 5종의 아크릴 변성 올리고머의 점도는 대표적인 광경화 가교제인 DPHA의 1/4 정도인 702-1250 cPs로 관찰되었다. 합성한 아크릴 변성 올리고머가 포함된 광경화 수지에 50초 이상 충분한 UV를 조사 시 DPHA를 포함하는 수지와 비슷한 경화도를 가지는 광경화 시편을 얻을 수 있었다. 각종 분석을 한 결과 DPHA를 사용한 광경화 시편보다 Tg, 연신율, 인장강도, 경도가 높은 것을 확인하였다. 그중 BA85/15를 이용하여 제작한 광경화 시편이 경화도 및 경도가 가장 우수한 것으로 관찰되었다. 이를 통해 본 연구에서 합성한 아크릴 변성 아크릴레이트 올리고머를 광경화 수지에 사용 시 점도 문제를 해결하고 고분자의 유연성을 증가시킬 수 있는 광경화 가교제로 적용 가능한 것으로 판단하였다.
- 1. Fouassier, J. P.; Rabek, J. F. Radiation Curing in Polymer Science and Technology: Fundamentals and Methods; Elsevier Applied Science: New York, 1993.
-

- 2. Dowling, J. P.; Pappas, P.; Monroe, B. Chemistry & Technology of UV & EB Formulation for Coatings, Inks & Paints; SITA Technology: New York, 1991.
- 3. Rabek, J. F. Mechanisms of Photophysical Processes and Photochemical Reactions in Polymers: Theory and Applications; John Wiley and Sons: New York, 1987.
-

- 4. Wei, J.; Jin, Y. Z. Photo-Curable Coating; Chemical Industry Press; New York, 2013.
- 5. Hong, J. H. UV Curing Coating; Chosun University Press: Korea, 2002.
- 6. Matyjaszewski, K.; Davis, T. P. Handbook of Radical Polymerization; John Wiley & Sons: New York, 2003.
-

- 7. Auer, L.; Clark, S.; Schwentenwein, M.; Gorsche, C.; Stampfl, J.; Liska, R. Toughening of Photo-curable Polymer Networks: A Review. Polym. Chem. 2016, 7, 257-286.
-

- 8. Kim, S. H.; Chang, H. S.; Park, S. H.; Song, K. G. Study on The Curing Properties of Photo-curable Acrylate Resins. Polym. Korea 2010, 34, 469-473.
-

- 9. Iijima, T.; Tomoi, M.; Suzuki, A. Toughening of Epoxy Resins by Modification with Reactive Elastomers Composed of Butyl Acrylate and Glycidyl (meth) Acrylate. Euro. Polym. J. 1991, 27, 851-858.
-

- 10. Wang, T.; Wang, J.; Chen, W.; Duan, H.; Xiao, H.; Wang, J.; Yang, J. Toughening Epoxy Resins by Modification with in situ Polymerized Acrylate Copolymer Composed of Butyl Acrylate and Glycidyl Methacrylate. High Perform. Polym. 2015, 27, 177-182.
-

- 11. Fuente, D. L.; Luis, J.; Cañamero, P. F.; García, M. F. Synthesis and Characterization of Glycidyl Methacrylate/Butyl Acrylate Copolymers Obtained at Low Temperature by Atom Transfer Polymerization. J. Polym. Sci. Part A: Polym. Chem. 2006, 44, 1807-1816.
-

- 12. Ludovic, V.; Massardier, V.; Pascault, J. P.; Magny, B. Synthesis and Photopolymerization of Acrylic Acrylate Copolymers. J. Appl. Polym. Sci. 2002, 86, 753-763.
-

- 13. Khafagi, M. G.; Salem, A. M.; Essawy, H. A. Synthesis and Optical Characterization of Poly(glycidyl methacrylate-co-butyl acrylate) Copolymers. Mater. Lett. 2004, 58, 3674-3680.
-

- 14. Lu, S.; Li, Y.; Zheng, J.; Lu, M.; Wu, K. Modified Epoxy Acrylate Resin for Photocurable Temporary Protective Coatings. Progress in Organic Coatings 2015, 89, 17-25.
-

- 15. Fage, J.; Knoll, K.; Niessner, N.; Carstensen, O.; Schulz, T.; Malz, F.; Döring, M.; Schönberger, F. Poly(Butyl Acrylate)-Graft-Polystyrene Synthesis by Free-Radical Polymerization: Interplay between Structure, Morphology, Mechanical, and Optical Properties. Polymers 2019, 11, 1317-1325.
-

- 16. Kunal, W.; Sabnis, A. Synthesis and Characterization of UV Oligomer Based on Cardanol. J. Renew. Mater. 2020, 8, 57-68.
-

- 17. Kim, J.-Y.; Moon, B.-J.; Kang, D.-W.; Hwang, S.-H. Synthesis and Cured Film Properties of UV-Curable Caprolactone-Modified Urethane Acrylate Oligomers. Polym. Korea 2010, 34, 574-578.
-

- 18. Jeong, E.-G.; Ryu, S.-W. Synthesis of Methacrylate Derivatives Based on Abietic Acid and Their Photo-curing Properties. Polym. Korea 2020, 44, 857-880.
-

- 19. Jinyue, D.; Liu, X.; Ma, S.; Wang, J.; Shen, X.; You, S. Soybean oil-based UV-curable Coatings Strengthened by Crosslink Agent Derived from Itaconic Acid Together with 2-Hydroxyethyl Methacrylate Phosphate. Progress in Organic Coatings 2016, 97, 210-215.
-

- 20. Bajpai, M.; Shukla, V.; Kumar, A. Film Performance and UV Curing of Epoxy Acrylate Resins. Progress in Organic Coatings 2002, 44, 271-278.
-

- Polymer(Korea) 폴리머
- Frequency : Bimonthly(odd)
ISSN 0379-153X(Print)
ISSN 2234-8077(Online)
Abbr. Polym. Korea - 2022 Impact Factor : 0.4
- Indexed in SCIE
 This Article
This Article
-
2022; 46(5): 543-550
Published online Sep 25, 2022
- 10.7317/pk.2022.46.5.543
- Received on Dec 23, 2021
- Revised on Mar 4, 2022
- Accepted on Jun 8, 2022
 Services
Services
Shared
 Correspondence to
Correspondence to
- Jinyoung Bae
-
Department of Polymer Science and Engineering, Sungkyunkwan University, 2066, Seobu-Ro, Jangan-Gu, Suwon-Si, Gyeonggi-Do 16419, Korea
- E-mail: b521@skku.edu
- ORCID:
0000-0002-9269-0322










 Copyright(c) The Polymer Society of Korea. All right reserved.
Copyright(c) The Polymer Society of Korea. All right reserved.